دی هیدروفولات ردوکتاز چیست و چه کاربردهایی دارد؟

دی هیدروفولات ردوکتاز یا DHFR، آنزیمی است که دی هیدروفولیک اسید را به اسید تتراهیدروفولیک کاهش می دهد. این تبدیل با استفاده از NADPH به عنوان دهنده الکترون صورت می گیرد که می تواند به انواع کوفاکتورهای تتراهیدروفولات مورد استفاده در شیمی انتقال تک کربن تبدیل شود.
DHFR عضوی از خانواده آنزیم ردوکتاز است که در همه موجودات بیان می شود و برای رشد و تکثیر سلولی حیاتی است. بنابراین DHFR هدفی برای عوامل درمانی ضد التهابی و ضد سرطانی است. یک مثال کلاسیک متوترکسات، آنالوگ فولات است که برای مهار DHFR استفاده می شود تا در نهایت از تکثیر لنفوسیت ها و سایر سلول های مسئول التهاب در مفصل جلوگیری کند.
در انسان آنزیم دی هیدروفولات ردوکتاز توسط ژن DHFR کدگذاری می شود که در ناحیه q11→q22 کروموزوم ۵ یافت می شود. گونه های باکتریایی دارای آنزیم های متمایز DHFR هستند (بر اساس الگوی اتصال مولکول های دی آمینو هتروسیکلیک)، اما DHFRهای پستانداران بسیار مشابه هستند. در ادامه مقاله در نشریه جهان شیمی فیزیک توضیحات بیشتری در رابطه با این آنزیم و کاربردهای آن ارائه می گردد لطفا همراه ما باشید.
ساختار آنزیم دی هیدروفولات ردوکتاز
دی هیدروفولات ردوکتاز (DHFR) یک آنزیم ضروری در بسیاری از موجودات است. این آنزیم کاهش وابسته به NADPH 7،۸-دی هیدروفولات (H2F) به ۵،۶،۷،۸-تتراهیدروفولات (H4F) را کاتالیز می کند. تتراهیدروفولات برای بسیاری از واکنش های انتقال تک کربن، به ویژه در تولید پورین ها، دئوکسی تیمیدین، گلیسین، متیونین و (در پروکاریوتها) اسید پانتوتنیک مورد نیاز است.
به این ترتیب، DHFR یک هدف دارویی مهم و یک هدف بالینی برای درمان های ضد باکتری، ضد مالاریا و ضد سرطان است. تقریبا تمام DHFR های کروموزومی شناخته شده آنزیم های مونومر هستند.
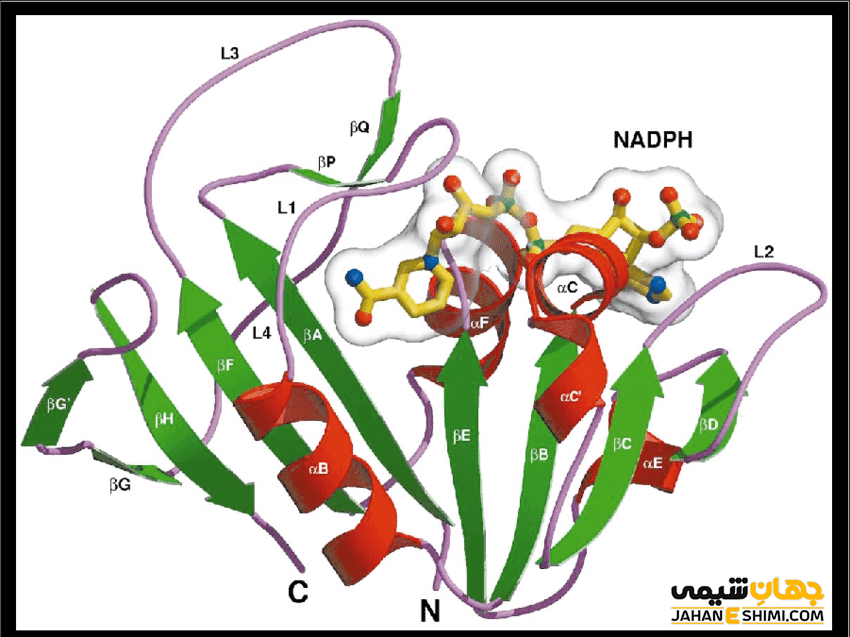
یک ورقه مرکزی هشت رشته ای بتای چین دار ویژگی اصلی تا خوردگی ستون فقرات پلی پپتیدی DHFR را تشکیل می دهد. هفت رشته از این رشته ها موازی و رشته هشتم غیر موازی است. چهار مارپیچ آلفا رشته های بتا متوالی را به هم متصل می کنند.
باقیماندههای ۹ تا ۲۴ «Met20» یا «حلقه ۱» نامیده می شوند و همراه با حلقه های دیگر، بخشی از زیر دامنه اصلی هستند که سایت فعال را احاطه کرده اند. سایت فعال در نیمه N ترمینال توالی قرار دارد که شامل یک دی پپتید Pro-Trp حفاظت شده است. تحقیقات نشان داده است که تریپتوفان در اتصال سوبسترا به آنزیم نقش دارد.
نحوه عملکرد دی هیدروفولات ردوکتاز
این آنزیم، دی هیدروفولات را به تتراهیدروفولات تبدیل می کند، یک شاتل پروتون که برای سنتز پورین ها، اسید تیمیدیلیک و اسیدهای آمینه خاص لازم است. در حالی که ژن عملکردی دی هیدروفولات ردوکتاز کروموزوم ۵ نگاشت شده است، چندین شبه ژن کاذب فرآوری شده بدون اینترون یا ژن های شبه دی هیدروفولات ردوکتاز بر روی کروموزوم های جداگانه شناسایی شده اند.
DHFR که در همه موجودات یافت می شود، نقش مهمی در تنظیم میزان تتراهیدروفولات در سلول دارد. تتراهیدروفولات و مشتقات آن مهمترین ترکیبات دخیل در سنتز پورین و تیمیدیلات هستند که برای تکثیر سلولی و رشد سلولی مورد نیازند. DHFR نقش اصلی را در سنتز پیش سازهای اسید نوکلئیک ایفا می کند و نشان داده شده است که سلول های جهش یافته که به طور کامل فاقد DHFR هستند برای رشد به گلیسین، یک اسید آمینه و تیمیدین نیاز دارند. DHFR همچنین به عنوان آنزیمی که در ساخت تتراهیدروبیوپترین از دی هیدروبیوپترین نقش دارد، شناخته شده است.
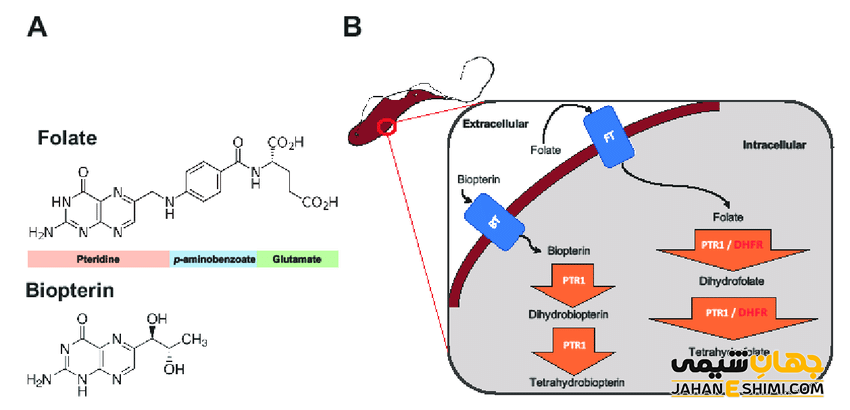
مکانیسم اثر دی هیدروفولات ردوکتاز
DHFR انتقال یک هیدرید از NADPH به دی هیدروفولات را همراه با پروتوناسیون برای تولید تتراهیدروفولات کاتالیز می کند. در نهایت دی هیدروفولات به تتراهیدروفولات احیا می شود و NADPH به NADP+ اکسید می شود. انعطاف پذیری بالای Met20 و سایر حلقه ها در نزدیکی محل فعال، در تسریع آزادسازی محصول، تتراهیدروفولات، نقش دارند. به ویژه حلقه Met20 به تثبیت حلقه نیکوتین آمید NADPH کمک می کند تا انتقال هیدرید از NADPH به دی هیدروفولات را افزایش دهد.
DHFR (حلقه Met20) + NADPH + فولات
مکانیسم این آنزیم به صورت گام به گام و تصادفی حالت پایدار است. به طور خاص، واکنش کاتالیزوری با اتصال NADPH و سوبسترا به محل اتصال آنزیم آغاز می شود و به دنبال آن پروتوناسیون و انتقال هیدرید از کوفاکتور NADPH به سوبسترا انجام می شود.
با این حال، دو مرحله اخیر به طور همزمان در یک حالت گذار انجام نمی شوند. در یک مطالعه با استفاده از رویکردهای محاسباتی و تجربی، لیو و همکاران به این نتیجه رسیدند که مرحله پروتوناسیون مقدم بر انتقال هیدرید است.
لازم به ذکر است که مکانیسم آنزیمی DHFR به ویژه مرحله انتقال هیدرید بسیار به Ph وابسته است. زیرا تغییرات pH تأثیر قابل توجهی بر الکترواستاتیک محل فعال و وضعیت یونیزاسیون باقیماندههای آن دارد. Asp27 تنها باقی مانده آبدوست باردار در محل اتصال است و خنثی سازی بار روی Asp27 ممکن است pKa آنزیم را تغییر دهد. Asp27 با کمک به پروتونه شدن بستر و مهار بستر در ترکیب مطلوب برای انتقال هیدرید، نقش مهمی در مکانیسم کاتالیزوری ایفا می کند.
نشان داده شده است که مرحله پروتوناسیون با توتومریزاسیون انول مرتبط است حتی اگر این تبدیل برای اهدای پروتون مطلوب در نظر گرفته نشود. ثابت شده است که یک مولکول آب در مرحله پروتونه شدن نقش دارد. همچنین مشخص شده است که ورود مولکول آب به محل فعال آنزیم توسط حلقه Met20 تسهیل می شود.
کاربردهای دی هیدروفولات ردوکتاز
دی هیدروفولات ردوکتاز یک آنزیم مهم در سنتز نوکلئیک و اسید آمینه و یک هدف دارویی است که در ۵۰ سال گذشته به طور گسترده مورد مطالعه قرار گرفته است. چالش های شیمی درمانی مبتنی بر مهار DHFR جدید برای درمان بیماری های عفونی اکنون بر روی غلبه بر مشکل مقاومت و همچنین مقرون به صرفه بودن متمرکز شده اند. هر سال، تعداد زیادی از مقالات علمی مستند به محبوبیت مداوم DHFR تأیید می کنند. DHFR واقعا یک آنزیم انتخابی برای تمام فصول و تقریبا همه بیماری ها است.
تتراهیدروفولات (THF) یک کوفاکتور ضروری متابولیسم تک کربنی است. به عنوان مثال، THF برای تبدیل هموسیستئین به اسید آمینه متیونین و برای بیوسنتز dTTP، یکی از چهار بلوک سازنده نوکلئوتیدی DNA، از dUTP مورد نیاز است. در این واکنش ها ابتدا تتراهیدروفولات متیله شده و سپس اکسیده می شود و به دی هیدروفولات تبدیل می شود. برای اجازه دادن به چرخه های متعدد، دی هیدروفولات باید دوباره کاهش یابد.
دی هیدروفولات ردوکتاز آنزیمی است که این امر را امکان پذیر می سازد. مانند بسیاری از کوفاکتورهای رایج، تتراهیدروفولات جدید در بدن انسان سنتز نمی شود. در عوض، آن را به عنوان ویتامین B9 در یک رژیم غذایی سالم، به عنوان مثال از طریق سبزیجات برگ دار (نام اسید فولیک از لاتین folio، برگ گرفته شده است) دریافت می کنیم.
بسیاری از کشورها مواد غذایی رایج مانند آرد را با ویتامین B9 (به شکل اسید فولیک) غنی می کنند تا سطح کافی این آنزیم را در رژیم غذایی را تضمین کنند. همانطور که در بالا توضیح داده شد، DHFR همچنین در کاهش اسید فولیک به تتراهیدروفولات فعال بیولوژیکی نقش دارد.
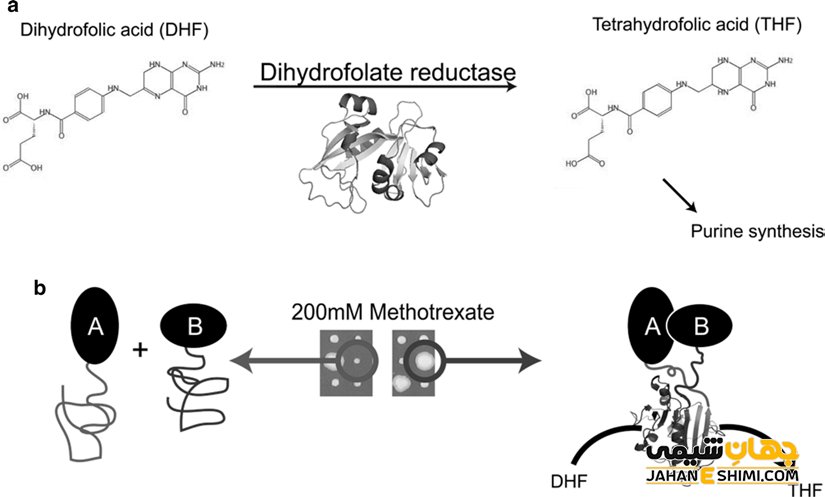
متوترکسات و دی هیدروفولات ردوکتاز
متوترکسات دی هیدروفولات ردوکتاز (DHFR) را مهار می کند، آنزیمی که اسید فولیک را به اسید تتراهیدروفولیک کاهش می دهد. تتراهیدروفولات باید از طریق واکنش کاتالیز شده با DHFR بازسازی شود تا مجموعه درون سلولی مشتقات تک کربنی تتراهیدروفولات برای بیوسنتز تیمیدیلات و نوکلئوتید پورین حفظ شود.
مهار DHFR توسط آنتاگونیست های فولات (متوترکسات) منجر به کمبود در سلولی تیمیدیلات و پورین ها و در نتیجه کاهش سنتز اسید نوکلئیک می شود. بنابراین، متوترکسات در سنتز DNA، ترمیم و تکثیر سلولی اختلال ایجاد می کند که در درمان سرطان مهم است.
متوترکسات بیشتر در برابر سلول هایی که به سرعت تکثیر می شوند فعال است، زیرا اثرات سیتوتوکسیک آن عمدتا در مرحله S چرخه سلولی رخ می دهد. از آنجایی که تکثیر سلولی در بافت های بدخیم بیشتر از اکثر بافت های طبیعی است، متوترکسات ممکن است رشد بدخیم را بدون آسیب غیر قابل برگشت به بافت های طبیعی مختل کند. در نتیجه، بافت های در حال تکثیر فعال مانند سلول های بدخیم، مغز استخوان، سلول های جنین، مخاط دهان و روده و سلول های مثانه به طور کلی نسبت به اثرات مهاری متوترکسات در مهار DHFR حساس تر هستند.
سمیت سلولی متوترکسات ناشی از سه عمل مهم است: مهار DHFR، مهار تیمیدیلات سنتاز و تغییر در انتقال فولات احیا شده. میل ترکیبی DHFR به متوترکسات بسیار بیشتر از میل ترکیبی آن برای اسید فولیک یا دی هیدروفولیک اسید است. بنابراین دوزهای زیاد اسید فولیک که به طور همزمان داده می شود، اثرات متوترکسات را معکوس نمی کند.
با این حال، لئوکوورین کلسیم، مشتق اسید تتراهیدروفولیک، ممکن است اثرات متوترکسات را در صورتی که مدت کوتاهی پس از داروی ضد نئوپلاستیک داده شود، مسدود کند. متوترکسات در دوزهای بالا و به دنبال آن لئوکوورین به عنوان بخشی از درمان بیماران مبتلا به استئوسارکوم غیر متاستاتیک استفاده می شود.
منطق اولیه برای درمان با دوز بالا متوترکسات بر مفهوم نجات انتخابی بافت های طبیعی توسط لوکوورین بود. شواهد جدیدتر نشان می دهد که دوز بالای متوترکسات همچنین ممکن است بر مقاومت متوترکسات ناشی از اختلال در انتقال فعال، کاهش میل ترکیبی دی هیدروفولیک اسید ردوکتاز برای متوترکسات، افزایش سطوح دی هیدروفولیک اسید ردوکتاز ناشی از تقویت ژن، یا کاهش پلی گلوتامیناسیون متوترکسات غلبه کند.
متوترکسات دارای فعالیت سرکوب کننده سیستم ایمنی است که ممکن است در نتیجه مهار تکثیر لنفوسیت ها باشد. مکانیسم های اثر در مدیریت آرتریت روماتوئید دارو مشخص نیست، اگرچه مکانیسم های پیشنهادی شامل اثرات سرکوب کننده سیستم ایمنی و یا ضد التهابی است.
در پسوریازیس، سرعت تولید سلول های اپیتلیال در پوست نسبت به پوست معمولی بسیار افزایش می یابد. این تفاوت در نرخ تکثیر مبنایی برای استفاده از متوترکسات برای کنترل فرآیند پسوریازیس است که با مهار آنزیم DHFR صورت می گیرد.
اهمیت دی هیدروفولات ردوکتاز در پزشکی
آنزیم هایی که در بدن نقش های اساسی دارند اهداف حساسی برای درمان دارویی هستند. دی هیدروفولات ردوکتاز اولین آنزیمی بود که برای شیمی درمانی سرطان هدف قرار گرفت. اولین دارویی که برای شیمی درمانی سرطان استفاده شد آمینوپترین بود. این ماده هزار بار محکم تر از فولات به دی هیدروفولات ردوکتاز متصل می شود و از عملکرد آنزیم جلوگیری می کند.
امروزه، متوترکسات و سایر انواع آمینوپترین به دلیل اتصال محکم تر و ویژگی های بالینی بهتر در درمان سرطان مورد استفاده قرار می گیرند. از آنجایی که این داروها به یک مرحله کلیدی در تولید DNA حمله می کنند، تمایل دارند سلول هایی را که به طور فعال در حال رشد هستند را از بین ببرند تا سلول هایی که در حال رشد نیستند.
از آنجایی که سلول های سرطانی اغلب سریع ترین سلول هایی هستند که در بیمار تکثیر می شوند، دارو قوی ترین اثر را روی سلول های سرطانی خواهد داشت. با این حال، عوارض جانبی شیمی درمانی، نتیجه دارو بر روی سایر بافت های در حال رشد طبیعی مانند فولیکول های مو و پوشش معده است.
DHFR یک آنزیم حیاتی چرخه فولات است که توسط داروهای ضد فولات مورد استفاده در درمان سرطان و آرتریت روماتوئید استفاده می شود. تغییر در بیان و فعالیت DHFR ناشی از پلی مورفیسمهای ژنتیکی ممکن است بر استعداد فرد برای پاسخ به درمان از نظر اثربخشی و عوارض جانبی دارو تأثیر بگذارد. با توجه به نقش مهم DHFR در تبدیل DHF به THF مورد نیاز برای سنتز اسید نوکلئیک و واکنش متیلاسیون، پلی مورفیسم های ژن DHFR ممکن است بر بیماری های وابسته به وضعیت فولات، مانند سرطان و اسپینا بیفیدا تاثیر بگذارد.
مزایای استفاده از دی هیدروفولات ردوکتاز
داروی متوترکسات برای تقلید از مولکول فولات طراحی شده است، به طوری که به محل فعال آنزیم متصل می شود و عملکرد آن را مسدود می کند. متوترکسات تقریبا به اندازه فولات است و ترکیب شیمیایی مشابهی دارد. محققان تائید کردند که این دارو در واقع عمل فولات را تقلید می کند و در موقعیت بسیار مشابهی متصل می شود. در طی واکنش شیمیایی، اتم های هیدروژن از نیکوتین آمید به این حلقه های بزرگ و مسطح منتقل می شوند.
دی هیدروفولات ردوکتاز در همه ارگانیسم ها استفاده می شود، اما هر ارگانیسم نسخه کمی متفاوت دارد. در طول تکامل دی هیدروفولات ردوکتاز به آرامی جهش یافته است و تغییرات کوچکی ایجاد شده است اما عملکرد اصلی را ثابت نگه می دارد. نسخه باکتری کوچک تر و ساده تر از نسخه موجود در سلول های انسانی است. محققان داروهایی ساخته اند که از تفاوت ها استفاده می کنند. به عنوان مثال، داروی تری متوپریم حدود ۳۰۰۰۰ برابر محکم تر به آنزیم باکتری متصل می شود. بنابراین، به عنوان یک داروی آنتی بیوتیک موثر است. دوز کم تری متوپریم به باکتری ها حمله می کند در حالی که دی هیدروفولات ردوکتاز در سلول های انسانی نسبتا دست نخورده باقی می ماند.