هیدروکربن های آروماتیک – خصوصیات و ویژگی ها
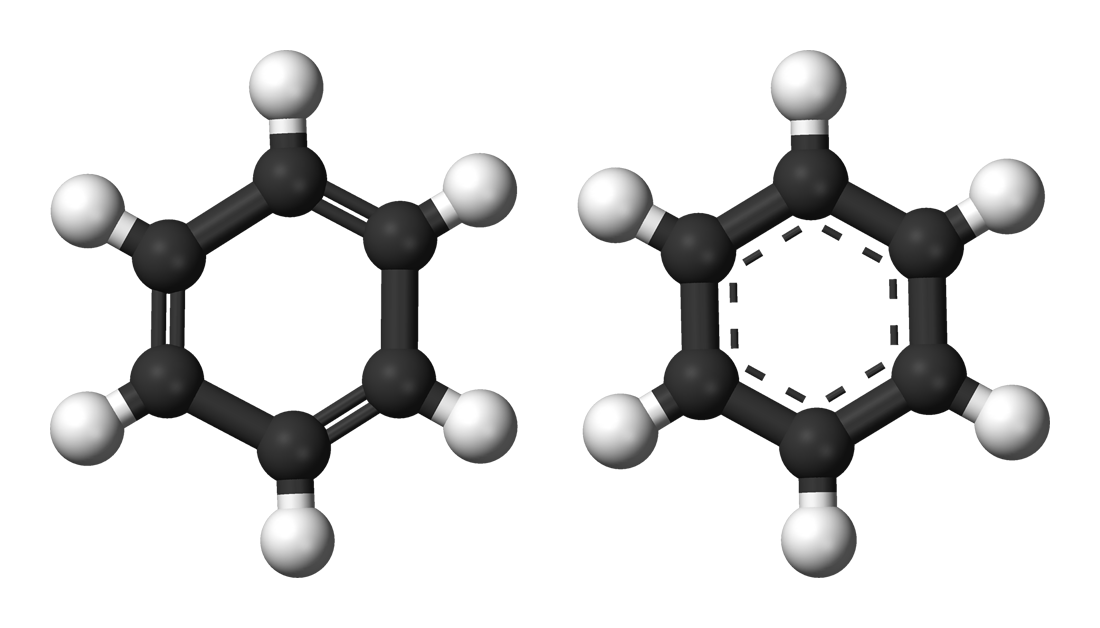
هیدروکربن های آروماتیک یا حلقوی در واقع دسته وسیعی از ترکیبات آلی را شامل میشوند. این ترکیبات ساختاری حلقوی و مسطح دارند و دارای پیوند های دوگانه (پای π) و یگانه (سیگما σ) میباشند. فرمول شیمیایی این ترکیبات به صورت CnHn است. این ترکیبات با وجود درجه غیر اشباعی بالا (به دلیل وجود الکترون های π زیاد در سیستم) پایدارند و مقاومت زیادی را نسبت به انجام واکنش های افزایشی نشان میدهند.
دلیلی که به این ترکیبات آروماتیک یا حلقوی می گویند این است که کلمه آروماتیک به معنی بوی خوش و معطر است. بسیاری از این ترکیبات، بوی شیرین و معطری را به مشام می رسانند. البته باید توجه داشت که تمامی ترکیبات آروماتیک، بوی شیرین و معطری ندارند و الزاما اگر ترکیبی بوی شیرین داشت در دسته ترکیبات آروماتیک قرار نمی گیرد. در ادامه مقاله در نشریه جهان شیمی فیزیک توضیحات بیشتری در این رابطه ارائه می شود. لطفا با ما همراه باشید.
خصوصیات و ویژگی های آروماتیک
مهمترین سوالی که در ابتدا با آن مواجه میشویم این است که اصلا ترکیب آروماتیک چیست؟ یک ترکیب آروماتیک، ترکیبی است که از قاعدهی هوکل پیروی کند. بنابراین این ترکیبات باید سه شرط زیر را داشته باشند:
۱- سیستم حلقوی باشد. تمام یا قسمتی از آن ترکیب حتما مسطح بوده و همچنین الکترون های π آن، در رزونانس کامل باشند.
۲- هیبرید اتم های کربن در ترکیب آروماتیک، sp² باشد.
۳- تعداد الکترون های شرکت کننده در رزونانس، از قاعده ۲n+4 که n در آن ۰، ۱، ۲، ۳ و …. است (قاعده هوکل) پیروی کنند
هتروسیکل های آروماتیک
ترکیب هتروسیکل آروماتیک چیست؟ اگر به تعریف ترکیبات آروماتیک دقت کنید، متوجه میشوید که هیچ کجا گفته نشده که تمام اتم های یک ترکیب آروماتیک باید حتما کربن باشند. بنابراین اتم های اکسیژن، نیتروژن، گوگرد و یا حتی سایر عناصر نیز میتوانند در ساختار حلقه قرار بگیرند. در واقع هترواتم ها، اوربیتال های خالی و یا جفت الکترون های غیر پیوندی خود را در رزونانس حلقه شرکت داده و ترکیبات آروماتیک ایجاد می کنند.
این ترکیبات، با نام هتروسیکل های آروماتیک شناخته میشوند. یکی از مشهور ترین حلقه های این دسته از ترکیبات، پیریدین (Pyridine) است. پیریدین ساختاری شبیه به حلقه ی بنزن دارد و تنها تفاوتشان در اینست که اتم نیتروژن در حلقه شش عضوی، جایگزین یک گروه CH شده است. نکته قابل ذکر اینست که الکترون های غیر پیوندی اتم نیتروژن، در رزوناس حلقه شرکت نمی کنند اما سه جفت الکترون π در رزونانس حلقه مشارکت دارند. بنابراین حلقه از قاعده هوکل پیروی می کند.
در جملات بالا درباره هیدروکربنهای آروماتیک و هتروسیکل های آروماتیکی که دارای حلقه های شش عضوی بودند صحبت کردیم. اما با توجه به تعریف آروماتیسیته، لزومی ندارد که ترکیب مورد نظر حتما دارای حلقه بنزنی باشد. به آن دسته از ترکیبات آروماتیک که از قانون هوکل پیروی می کنند اما در ساختار خود حلقه بنزن ندارند، هتروآرن (Heteroarenes) می گویند. در این ترکیبات، اگر فقط یک اتم کربن با یک هترواتم جایگزین شود، هتروآرن هایی به نام های فوران (شامل اکسیژن)، پیرول (شامل نیتروژن) و تیوفن (شامل گوگرد) تشکیل می¬شوند.
دسته بندی هیدروکربن های آروماتیک
تقسیم بندی هیدروکربن های آروماتیک بستگی به تعداد حلقه ها دارد. بنابراین این ترکیبات به دو دسته تک حلقهای یا مونو سیکلیک (Monocyclic Aromatic Hydrocarbon) که به طور مختصر با (MAH) و چند حلقهای یا پلی سیکلیک (Polycyclic Aromatic Hydrocarbon) که به اختصار با (PAH) نشان داده میشوند تقسیم می گردند.
هیدروکربن های آروماتیک تک حلقهای
ساده ترین و مهم ترین هیدروکربن آروماتیک تک حلقهای، بنزن است. ساختار بنزن با فرمول شیمیایی C6H6، اولین بار توسط ککوله بیان شد. او دو ساختار که در محل قرار گرفتن پیوند های π با یکدیگر فرق دارند پیشنهاد داد. بعد از آن، دانشمندان بر اساس شواهد بدست آمده و بررسی های انجام شده ساختار رزونانس را برای حلقه بنزن پیشنهاد دادند. در این ساختار، بنزن به صورت یک شش ضلعی با یک حلقه در درون آن نشان داده می شود. این حلقه مرکزی تعداد الکترون ها را مشخص نمیکند اما یکسان بودن پیوندهای کربن-کربن را نمایش می دهد.
هیدروکربن های آروماتیک چند حلقهای
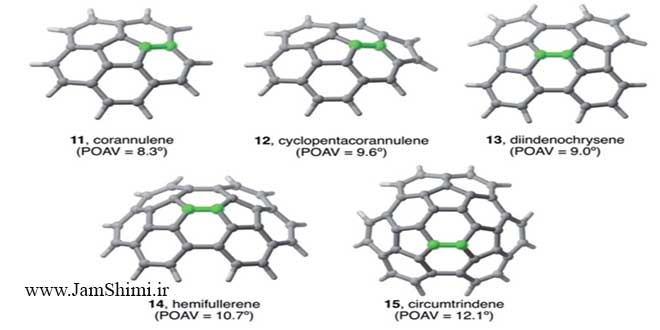
هیدروکربن های آروماتیک چند حلقهای، به گروهی از هیدروکربن های آروماتیک که از دو یا چند حلقه آروماتیک جوش خورده تشکیل شده باشند گفته میشود. بنابراین قاعدتا، در ساختار این هیدروکربن ها، چند اتم کربن مشترک وجود دارد. در ساختار این ترکیبات پلی سیکلیک آروماتیک، تنها اتم های کربن و هیدروژن وجود دارد، بنابراین قاعدتا بسیاری از خواص شیمیایی حلقه بنزن را نشان می دهند.
یکی از ساده ترین و مشهورترین ترکیب در گروه هیدروکربن های آروماتیک پلی سیکلیک، نفتالین است که از جوش خوردن دو حلقه بنزن تشکیل شده است. بنابراین نفتالین هم مانند بنزن دارای ساختار رزونانسی می باشد. برای آشنایی بیشتر با نفتالین میتوانید به مقاله آشنایی با کاربردهای گسترده و جالب نفتالین در نشریه جهان شیمی فیزیک رجوع نمایید.
این دسته از هیدروکربن ها را می توان به دو دسته سبک (۲ تا ۳ حلقه) و سنگین (۴ حلقه و بیشتر از آن) طبقه بندی کرد. اين هیدروکربن ها حلاليت كمي در آب دارند، اما در حلال های آلی بهتر حل می شوند. از طرفی، با افزایش تعداد حلقه ها، حلالیت کاهش مییابد. متاسفانه بسیاری از ترکیبات هیدروکربن های آروماتیک چند حلقه ای سمی و سرطان زا میباشند و خطری جدی برای سلامتی انسان ایجاد می کنند. متاسفانه این ترکیبهای چند حلقهای آروماتیک هم در منابع طبیعی وجود دارند و هم از طریق انسان به محیط اضافه می-شوند.
ترکیبات آنتی آروماتیک یا غیر آروماتیک
غیر از هیدروکربن های آروماتیک، ترکیبات آنتی آروماتیک یا غیر آروماتیک نیز وجود دارند. تعداد الکترون های π مزدوج در ترکیبات آنتی آروماتیک به صورت n4 است، که n در آن عددی مثبت و غیر صفر می باشد. در واقع، ترکیبات آنتی آروماتیک می توانند تمام شرایط یک ترکیب آروماتیک را داشته باشند، اما فقط تعداد الکترون های π مزدوج در آنها از قاعده هوکل پیروی نکند.
بنابراین اگر یک ترکیب حلقوی، مسطح و ظاهر مزدوج داشته باشند میتواند آروماتیک نباشد. توجه داشته باشید که اگر در سیستمی، الکترون های π به صورت مستقر وجود داشته باشند و در رزونانس شرکت نکنند (در واقع ترکیب فاقد پیوند π مزدوج باشد)، سیستم غیر آروماتیک است. این ترکیبات به دلیل ناپایداری، به شدت واکنش پذیرند.
خواص و ویژگی های هیدروکربن های آروماتیک
از جمله ویژگی های هیدروکربن های آروماتیک میتوان به موارد زیر اشاره کرد:
۱- هیدروکربن های آروماتیک در دسته مواد خوشبو و معطر قرار می گیرند.
۲- این ترکیبات خصلت آروماتیک دارند.
۳- گرمای سوختن و گرمای هیدروژن دار شدن پایینی دارند.
۴- نسبت اتم های کربن- هیدروژن در این ترکیبات بالاست.
۵- تمایل زیادی برای شرکت در واکنش های افزایشی نشان نمی دهند. اما در واکنش های جانشینی شرکت میکنند.
۶- در هنگام سوختن، به سرعت با اکسیژن واکنش داده و علاوه بر تولید آب و اکسید های کربن، انرژی به صورت گرما و نور (شعلهای زرد رنگ و همراه با دوده) آزاد می کنند.
۷- هرچه تعداد الکترون های شرکت کننده در رزونانس، بیشتر باشد، پایداری نسبی بالاتر است.
واکنش ها در هیدروکربن های آروماتیک
همان طور که در ابتدای این مقاله بیان شد، هیدروکربن های آروماتیک با وجود سیر نشده بودن، ترکیباتی بسیار پایدارند. بنابراین، تمایلی به شرکت در واکنش های افزایشی ندارند. مهمترین واکنش هایی که هیدروکربن های آروماتیک در آن شرکت میکنند، واکنش های جانشینی است. واکنش های جانشینی را میتوان به دو دسته واکنش های جانشینی آروماتیک هسته دوست (نوکلئوفیلی) و واکنش های جانشینی آروماتیک الکترون دوستی (الکتروفیلی) طبقه بندی کرد.
در واکنش های جانشینی الکترون دوستی آروماتیک، اتم هیدروژن در ساختار حلقه آروماتیک با اتم ها یا گروه های دیگر جایگزین میشود. از جمله این واکنش ها می توان به هالوژندار کردن (هالوژناسیون)، نیترودارکردن (نیتراسیون)، سولفوندارکردن (سولفوناسیون)، آلکیل دار کردن فریدل-کرافتس (آلکیلاسیون) و آسیل دار کردن فریدل-کرافتس (آسیلاسیون) اشاره کرد.
در واکنش های جانشینی هسته دوستی آروماتیک، یک گروه ترک کننده (مانند یک هالید) در ساختار حلقه آروماتیک با یک عامل هسته دوست جایگزین می شود. همانطور که مشخص است، هیدروکربن های آروماتیکی که بر روی حلقه آروماتیک خود دارای استخلاف الکترون کشنده باشند می توانند واکنش جانشینی هسته دوستی آروماتیک را انجام دهند.
توجه داشته باشید که اگر بخش حلقوی هیدروکربن های آروماتیک، دارای زنجیر جانبی آلکیلی باشد، این زنجیره می تواند در حضور اکسید کننده های قوی، اکسید شود. از طرفی، واکنش های رادیکالی جانشینی بر روی زنجیر جانبی آلکیلی هیدروکربن های آروماتیک امکان پذیر است. علاوه بر واکنش های جانشینی بیان شده در بالا، هیدروکربن های آروماتیک میتوانند در هیدروژناسیون و واکنش های کوپلینگ (مزدوج شدن یا جفت شدن) نیز شرکت کنند.
نکته قابل توجه در هیدروژناسیون این است که، بخش آلیفاتیک سیستم راحت تر از بخش حلقوی آن وارد واکنش هیدروژناسیون میشود. هیدروژناسیون بخش آروماتیک نیازمند دما و فشار بالاتری میباشد. محصول هیدروژناسیون ترکیبات آرن، حلقه های سیرشده است.
واکنش کوپلینگ چیست؟
به متصل شدن دو ماده ی اولیه ی هیدروکربنی با کمک یک کاتالیزور فلزی کوپلینگ می گویند که محصول واکنش یه ساختار واحد میباشد. واکنشهای کوپلینگ را بر اساس نوع مواده اولیه و کاتالیزور استفاده شده به دو دسته ی کوپلینگ جور (Homocoupling) و کوپلینگ ناجور یا متقاطع (Heterocoupling or Cross-coupling) تقسیم میکنند. در اثر شرکت هیدروکربنهای آروماتیک در واکنش های کوپلینگ سه نوع پیوند کربن-کربن، کربن-اکسیژن و کربن-نیتروژن تشکیل میشود.
کاربرد های هیدروکربن های آروماتیک
بسته به نوع هیدروکربن های آروماتیک، این دسته از مواد کاربردهای زیادی در زندگی انسان دارند. اما سوال مهم این است که مهمترین کاربرد هیدروکربن های آروماتیک چیست؟ باید بدانید که از این ترکیبات به طور عمده به عنوان سوخت استفاده می شود. همچنین از بیشتر هیدروکربن های آروماتیک سنگین در صنایع رنگ و رزین (به عنوان حلال) استفاده میکنند. نکته جالب توجه اینجاست که هیدروکربنهای آروماتیک حتی در بدن انسان نیز (نوکلئیک اسیدها و آمینو اسیدها) وجود دارند.
در ادامه مقاله چند نمونه دیگر از سایر کاربردهای هیدروکربن های آروماتیک بیان شده است. به عنوان مثال می توان به کاربرد این ترکیبات در سنتز داروها، صنایع غذایی، روان کننده ها، حلال ها، جوهر چاپ، فیبرها، چسب ها، ضد عفونی کننده ها، ضد کپک ها، گندزدا ها، حشره کش ها، ماده اولیه در ساخت فوم و پلاستیک، درزگیرهای سیلیکونی، تولید ماده اولیه الیاف مصنوعی، تولید ماده اولیه پلی استرها، ماده اصلی در ساخت مواد منفجره (TNT)، مدارهای الکترونیکی، سنسورهای صنعتی، صنایع خودروسازی، جلوگیری کننده از بید زدن لباسها، فرش ها و همچنین پارچه های پشمی و سایر مواد شیمیایی اشاره کرد.
نامگذاری هیدروکربن های آروماتیک
نامگذاری هیدروکربن های آروماتیک چگونه انجام میشود؟ هیدروکربن های آروماتیک نسبت به سایر مواد آلی داراي نام هاي متداول تری میباشند. بنابراین نامگذاری این ترکیبات به طور کامل از قواعد آیوپاک پیروی نمیکند. اگر ترکیب مورد نظر همزمان دارای قسمت های غیر حلقوی و حلقوی است و بخش غیر حلقوی ترکیب کوچکتر از بخش حلقوی آن باشد، بخش حلقوی به عنوان قسمت اصلی و بخش غیر حلقوی به عنوان استخلاف یا شاخه در نظر گرفته میشود.
اگر هیدروکربن آروماتیک تنها شامل یک حلقه بنزن تک استخلافی باشد، کلمه بنزن به عنوان نام اصلی استفاده میشود. در واقع در این حالت، نام گروه یا استخلاف حلقه به صورت پیشوند قبل از کلمه بنزن نوشته میشود (مثلا نیتروبنزن). حال اگر دو استخلاف داشته باشیم، برای نشان دادن محل قرار گرفتن استخلاف ها از پیشوند های اورتو، متا یا پارا استفاده میکنیم. جهت نامگذاری مشتقات سه استخلافی بنزن لازم است که از شماره برای ذکر موقعیت استخلاف ها استفاده شود. توجه داشته باشید که در هنگام نامگذاری ترکیبات سه استخلافه باید کوچکترین عدد هاي ممکن به استخلاف ها برسد و همچنین ترتیب الفبایی نام استخلاف ها رعایت شود.
اگر خود حلقه بنزن در ساختار به صورت استخلاف باشد، در نامگذاری ترکیب از کلمه فنیل استفاده میگردد. همچنین، برخی از مشتقات بنزن، نام مخصوصی داشته و به آن نام مشهورند. به عنوان مثال هیدروکسی بنزن را با نام فنل یا متیل بنزن را با نام تولوئن می شناسیم.
ترکیبات آروماتیک
ترکیبات معطر یا آروماتیک، یک کلاس مواد در شیمی آلی هستند که به دلیل بوی معطری که ترکیبات اولیه کشف شده از این طبقه را با آن شناسایی کردند، نامگذاری شده است. علاوه بر ترکیبات کربن حلقه ای شکل، مجتمع های فلزی معطر نیز شناخته شده اند که به موجب آن اتم فلز به یک مولکول آلی معطر متصل می شود. حلقه فلزی توصیف شده توسط شیمیدانان دانشگاه هایدلبرگ متفاوت است. این ماده تنها از اتم های فلزی بیسموت عنصری تشکیل شده است. جداسازی و خصوصیات این حلقه فلزی با رویکرد جدیدی از تثبیت فوق مولکولی امکان پذیر شد.
ترکیبات آروماتیک یا هیدروکربن های معطر دسته ای از هیدروکربن ها هستند که حداقل دارای یک حلقه معطر هستند. این ترکیبات به دلیل ساختارهای مولکولی حلقه مانند پایدار خود که دارای الکترون های پی غیرمحلی در سراسر سیستم مزدوج اتم ها هستند، شناخته شده اند. تعریف ترکیبات آروماتیک ساختار آنها را به عنوان مولکول های حلقه ای شکل با الکترو نهای غیرمحلی در میان پیوندهای دوگانه و منفرد متناوب برجسته می کند که به طور قابل توجهی پایداری شیمیایی آنها را افزایش می دهد. ترکیبات معطر شامل ترکیبات حلقه ای شکل هستند که به عنوان آرن یا آروماتیک نیز شناخته می شوند.
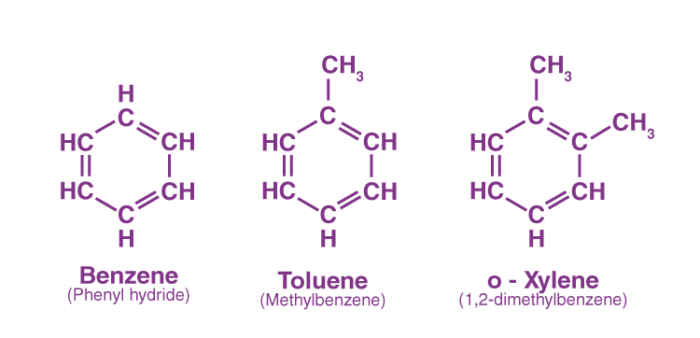
آنها دسته ای از ترکیبات شیمیایی هستند که با ساختار مولکولی حلقه ای شکل پایدار خود که شامل الکترون های غیرمحلی شده است مشخص می شوند. این الکترون ها معمولاً روی یک سیستم مزدوج از پیوندهای دوگانه و منفرد متناوب به اشتراک گذاشته می شوند و به مولکول اجازه می دهند به دلیل رزونانس پایداری بالاتری داشته باشند. مفهوم معطر بودن برای درک شیمی این ترکیبات است. نمونه های ترکیبات معطر عمدتاً شامل بنزن، تولوئن، زایلن است.



















