معادله یونش اسید فرمیک چیست؟

اسید فرمیک یا جوهر مورچه، اسیدی ضعیف با فرمول مولکولی HCOOH است. در نیش حشراتی چون مورچه و زنبور می توان به صورت طبیعی، این اسید ضعیف را مشاهده کرد. علت نام گذاری آن به نام جوهر مورچه نیز همین است. اسید فرمیک مانند بسیاری از اسیدهای دیگر وقتی در آب قرار می گیرد، به یون های سازنده خود تجزیه می شود. معادله یونش اسید فرمیک نیز با توجه به این خاصیت نوشته می شود. این مقاله نشریه جهان شیمی فیزیک نیز ما را با معادله یونش اسید فرمیک، ثابت تفکیک و قدرت تفکیک آن آشنا می کند.
فهرست مطالب
اسید فرمیک چیست؟
ساده ترین اسید کربوکسیلیک، اسید فرمیک است که برای اولین بار با تقطیر تخریبی مورچه به دست آمده است. این کار توسط جان ری، طبیعت شناس انگلیسی در سال ۱۶۷۱ صورت گرفت. اسید فرمیک قابل سنتز نیز است که اولین بار سنتز آن توسط ژوزف گیلوساک، شیمیدان فرانسوی انجام شد. سنتز اسید فرمیک از مونوکسید کربن برای اولین بار در سال ۱۸۵۵ به وسیله شیمیدان فرانسوای دیگری به نام Marcellin bertilot انجام شد.
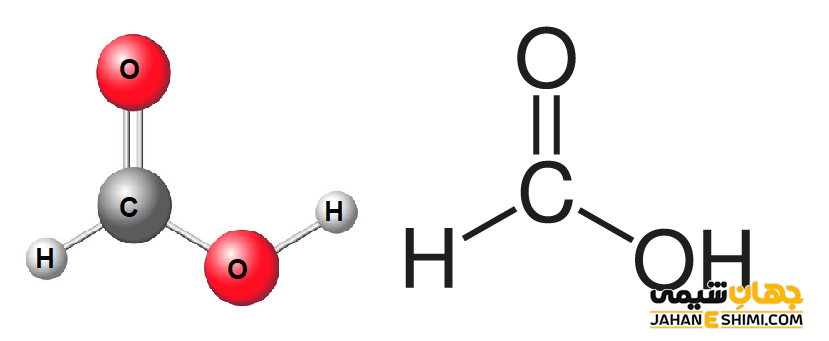
خواص اسید فرمیک
اسید فرمیک اسیدی ضعیف قابل حل در آب و اکثر حلال های قطبی است. حتی این اسید توانایی حلالیت در هیدروکربن ها را نیز به حد کمی دارد. از خواص اسید فرمیک در حالت گازی می توان به برقراری پیوند هیدروژنی میان مولکول های آن و تشکیل دیمرها در حالت گازی اشاره کرد. این خاصیت باعث می شود که این اسید در حالت گازی از قانون گازهای ایده آل پیروی نکند. اما در حالت مایع و جامد، این اسید به صورت شبکه ای محدود است که مولکول های آن با پیوند هیدروژنی با هم در اتصال هستند.
اگر اسید فرمیک گرما داده شود، تجزیه شده و تولید مونوکسید کربن می کند. از واکنش های دیگر این اسید، احیا است که فرمالدهید تشکیل می شود. در واکنش های افزایشی در کنار آلکن ها، فقط اسید فرمیک شرکت می کند. وقتی این اسید در برابر اسید سولفوریک و اسید هیدروفلوئوریک قرار می گیرد، تولید اسیدهای کربوکسیلیک بزرگتر می کند.
ثابت تفکیک چیست؟
برای اندازه گیری کمی قدرت اسیدی در یک محلول تابعی به نام ثابت تفکیک تعریف می شود که با K نمایش داده می شود. به عبارتی این ثابت می تواند قدرت نسبی یک اسید را در یک محلول بیان کند. معادله ای هم که برای بیان ثابت تفکیک اسید به کار می رود، به نام ثابت یونش اسید خوانده می شود. اسیدها وقتی در آب قرار می گیرند، یونیزه شده و به یون های تشیکیل دهنده خود تفکیک می شوند. در اسیدها یکی از یون های تشکیل شده، یون هیدروژن (H+) است. هر چه میزان تفکیک شدن اسید در آب بالاتر باشد و تولید یون های هیدروژن مثبت بیشتری کند، قدرت اسیدی آن نیز بیشتر خواهد بود.

معادله یونش اسید فرمیک
با توجه به تعریف ثابت تفکیک می توان معادله یونش اسیدها را به صورت زیر نوشت.
HA(aq) + H۲O(l) ↔ H۳O+ + A–(aq)
برای نوشتن ثابت یونش اسید نیز داریم :
K = [H۳O+][A–] / [H۲O][HA]
باید در معادله ثابت تفکیک اسیدها به این موضوع توجه کرد که غلظت آب خالص مقدار ثابتی بوده و در این معادلات با کمیت جدیدی به نام ثابت یونش اسید تعریف می شود.
Ka = K[H۲O]
در نتیجه با این تعریف معادله یونش اسیدها به صورت زیر نوشته می شود.
Ka = K[H۲O] = [H۳O+][A–] / [HA]
یون هیدروژن مثبت در آب به صورت آزاد نبوده و در ترکیب با مولکول های آب و به صورت یون هیدرونیوم وجود دارد.
رابطه ای که برای بیان قدرت اسیدی با ثابت تفکیک اسید می توان گفت، با زیاد شدن مقدار Ka، غلظت یون هیدرونیوم و همچنین قدرت اسید بالا می رود.
ثابت تفکیک اسید بر اساس فعالیت یون های هیدروژن مثبت و هیدروکسید منفی
ثابت تفکیک اسیدها و بازها را می توان مانند بسیاری از ثابت های تعادل دیگر، بر اساس فعالیت و اکتیویته یون های H+ و OH– بیان کرد. اما بیان این مقادیر بدون واحد است.
معادله یونش اسید فرمیک
اسید فرمیک نیز مانند بسیاری از اسیدهای دیگر در آب به یون های تشکیل دهنده تفکیک شده و تولید یون های H+ و HCOO– را می کند. تجزیه این اسید ضعیف به میزان کمی بوده و می توان معادله مربوط به تفکیک آن را به صورت زیر نوشت.
HCOOH + H۲O ↔ HCOO– + H۳O+
K = [HCOO–][H۳O+] / [HCOOH]
مقدار ثابت تفکیک اسید فرمیک ۱.۷۸ ͯ ۱۰-۴ است. علت این که اسید فرمیک به عنوان اسیدی ضعیف تعریف می شود، همین مقدار کم ثابت تفکیک آن است.
pKa اسید فرمیک
بعد از این که معادله یونش اسید فرمیک بیان شده و رابطه ثابت تفکیک و مقدار عددی آن گفته شد، می توان مقدار عددی ثابت تفکیک را با گرفتن لگاریتم از آن بیان کرد. بیان رابطه قدرت اسیدی با pKa به صورت زیر است.
pKa = -log ۱۰Ka
با توجه به این معادله هرچه مقدار pka کمتر باشد قدرت اسیدی بالاتر است. بر خلاف این که هرچه مقدار عددی ثابت تفکیک اسید بیشتر باشد، قدرت اسیدی بیشتر می شود.
کاربرد اسید فرمیک
یکی از مهمترین کاربردهای اسید فرمیک به عنوان نگهدارنده و آنتی باکتریال در ترکیب غذای دام ها و طیور است. با پاشیدن مقداری از این اسید ضعیف روی علف تازه خشک شده، از فاسد شدن آن جلوگیری می کنند. همچنین این اسید می تواند مواد مغذی علف ها را حفظ کند. به همین دلیل در دامداری های بزرگ از اسید فرمیک به عنوان عامل جلوگیری کننده فساد استفاده می کنند.
با کاربرد اسید فرمیک در مرغداری ها، باکتری سالمونلا که در غذای مرغ ها وجود دارد، از بین می رود. از کاربردهای دیگر این ماده در صنعت نساجی و دباغی است. صنعت خوشبوکننده ها نیز از مشتقات این اسید مانند استرهای فرمات استفاده می شود. اسید فرمیک در صنعت کشاورزی به عنوان یک آفت کش بسیار قوی به کار رفته و یک عامل ضد باکتری است. خاصیت ضد باکتریایی آن باعث می شود که تخمیر در سیلو در دمای پایین تری انجام شود. در عین حال که فواید مواد مغذی محصول زیاد می شود.
نکات ایمنی اسید فرمیک
مقدار مجاز اسید فرمیک در هوای محیط کار بر طبق اعلام سازمان غذا و داروی آمریکا، 5ppm گفته شده است. اگر پوست و چشم در تماس با اسید فرمیک غلیظ قرار گیرد، به این اعضا آسیب می زند. به طوری که پوست در تماس با بخارات و یا مایع این اسید، دچار سوختگی شیمیایی شده و تماس با چسم نیز می تواند باعث آسیب شود. اگر بخارات این اسید استشمام شود، تحریک و سوزش دستگاه تنفسی را سبب می شود.



















