آموزش کامل طیف اتمی از صفر تا صد – انواع طیف های اتمی
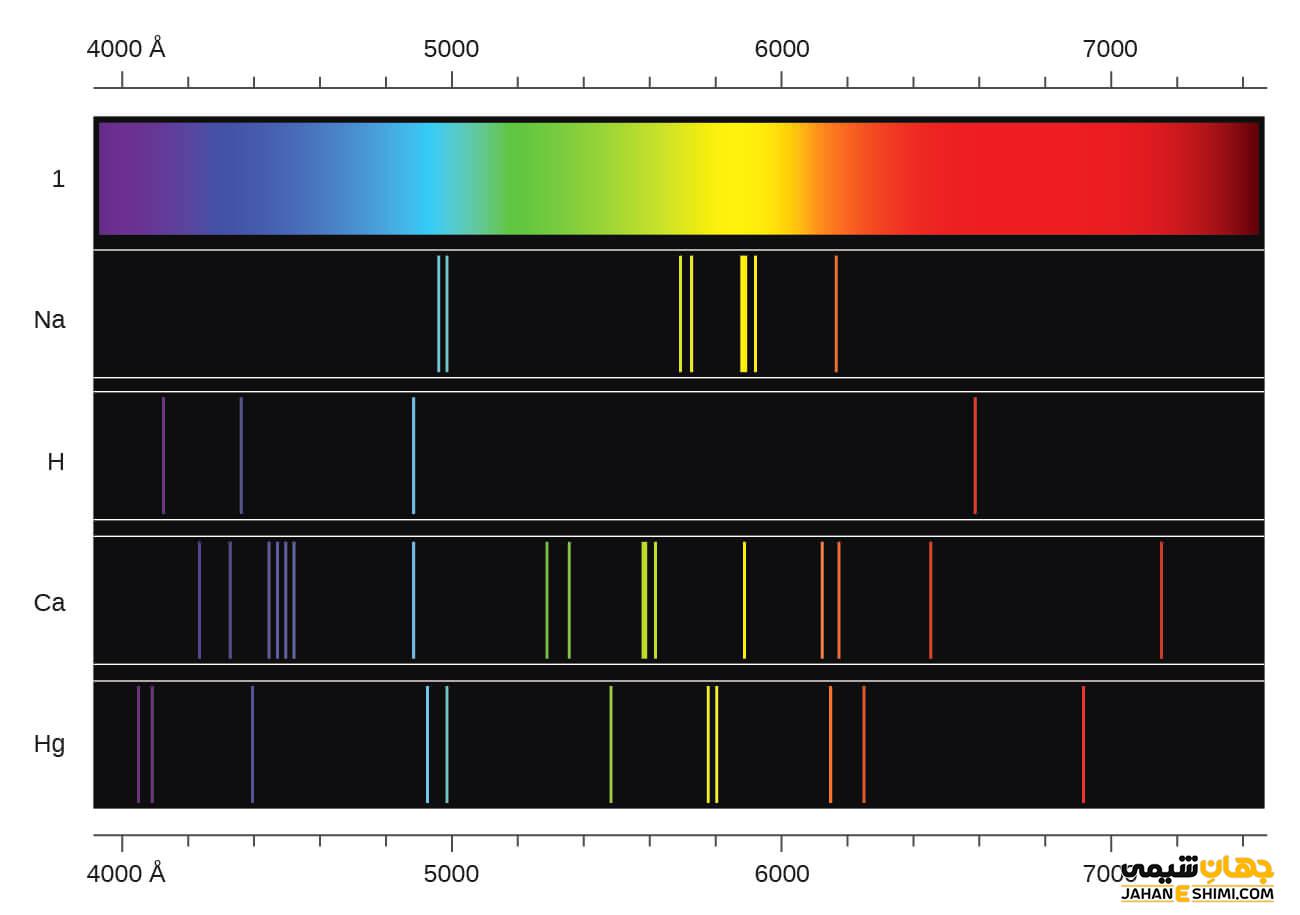
طیف اتمی روشی است که با آن می توان ترکیبات تشکیل دهنده یک جسم را تعیین و به شناسایی اتم مورد نظر پرداخت. طیف اتمی را با مجموعه ای از فرکانس ها و طول موج های مختلف، تعریف می کنند. روش ابتدایی برای به دست آوردن طیف یک جسم، عبور دادن نور از داخل یک منشور و تجزیه آن به خطوط طیفی مختلف است. این روش را طیف سنجی یا اسپکتروسکوپی می نامند. این مقاله نشریه جهان شیمی فیزیک ما را با طیف اتمی و انواع آن آشنا می کند.
فهرست مطالب
مقدمه ای بر مفهوم طیف اتمی
اولین بار نیوتن بود که با عبور نور خورشید از منشور، طیف نور سفید را تشکیل داد. او با این کار نشان داد که طیف نور سفید خورشید بین طول موج های ۰,۴ تا ۰,۷ میکرومتر قرار داشته و دارای رنگ های مختلفی است. طیف نور سفید پیوسته بوده و دارای رنگ های قرمز، نارنجی، زرد، سبز، آبی، نیلی و بنفش است. طول موج ۰,۴ میکرومتر مربوط به رنگ بنفش و طول موج ۰,۷ میکرومتر مربوط به رنگ قرمز است.
تعریف طیف اتمی
تابش امواج الکترومغناطیسی در یک محیط مادی و یا خلأ، به صورت موج عرضی و نوسانی متشکل از عمود بودن دو میدان الکتریکی و مغناطیسی بر هم است. وقتی موج های مغناطیسی در نتیجه عمود بودن میدان های الکتریکی و مغناطیسی در راستای محور x تشکیل می شوند، به فاصله دو موج از این نوسان، طول موج می گویند. میزان فشردگی این موج ها با کمیتی به نام فرکانس بیان می شود.
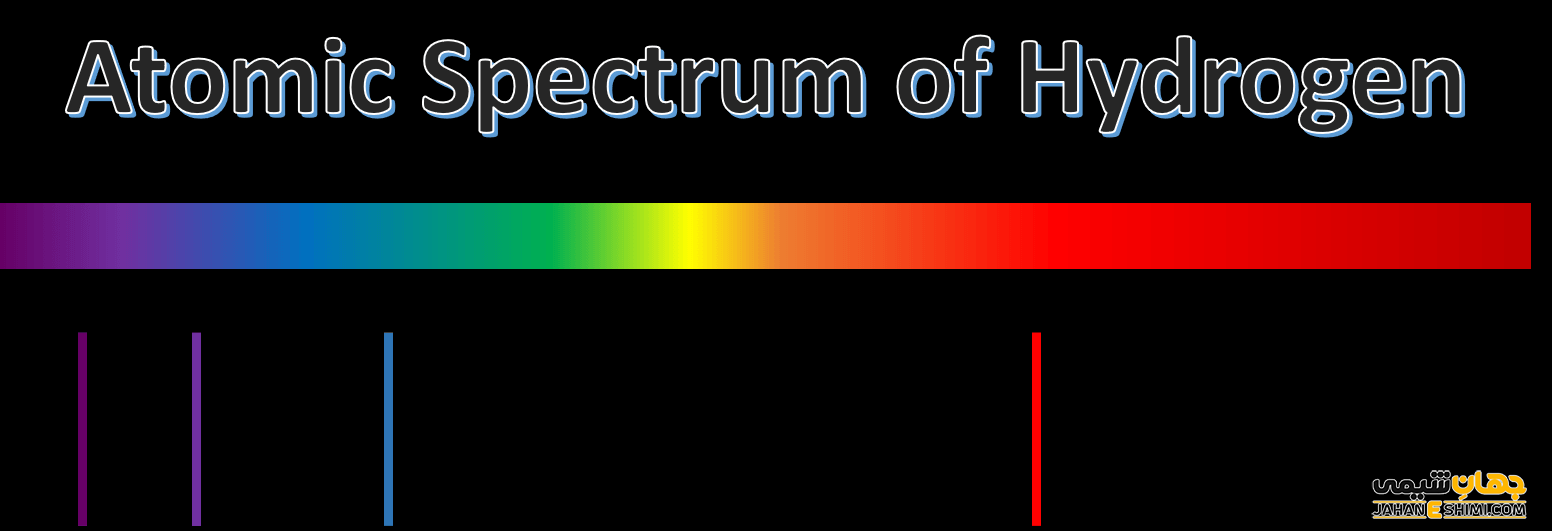
فرکانس در رابطه ای عکس با طول موج قرار دارد. هر چه موج فشرده تر باشد، میزان انرژی بزرگتری را تحمل کرده ولی طول موج کمتری خواهد داشت. موج الکترومغناطیسی در بازه ای از فرکانس ها و طول موج های تشکیل یافته انتشار پیدا می کند. به این بازه، طیف الکترومغناطیسی می گویند. در تعریف دقیق تر می توان گفت که فرکانس و طول موج های نشر شده و یا جذب شده، همان طیف اتمی هستند. نمونه ای از طیف اتمی که مربوط به اتم هیدروژن است، در شکل بالا نشان داده شده است.
تاریخچه کشف فوتون
موج الکترومغناطیسی را در برخی از تعاریف به عنوان ذره نیز در نظر می گیرند. این دیدگاه با توجه به تعریف الکترون به عنوان بیان کننده معنای دوگانگی موج – ذره، بر اساس مکانیک کوانتوم بیان می شود. در سال ۱۹۰۰ میلادی ماکس پلانک بیان کرد که وقتی فرکانس یک موجی افزایش پیوسته ای پیدا می کند، افزایش انرژی تابشی ایجاد شده پیوسته نیست. بلکه به شکل کوانتومی و پله ای و همچنین به شکل بسته های انرژی، انرژی تابشی افزایش می یابد. طوری که آلبرت انیشتین کسی بود که در سال ۱۹۰۵، این بسته های انرژی را به عنوان فوتون در نظر گرفت. با تعریف فوتون، زیاد شدن پله ای و کوانتومی بسته های انرژی نیز توضیح داده شد.
ثابت ها و واحدهای تعریف شده در طیف اتمی
طول موج : به فاصله میان دو قله یک موج، طول موج می گویند که بر حسب واحد متر، میکرومتر و یا نانومتر بیان می شود.
فرکانس : فرکانس موج به تعداد قله هایی از موج های الکترومغناطیسی گفته می شود که در مدت یک ثانیه، عبور می کنند. واحد فرکانس هرتز (Hz) یا بر ثانیه است. طول موج از تقسیم ثابت سرعت نور بر طول موج به دست می آید.
رابطه بین طول موج و فرکانس و سرعت نور

انرژی تابش الکترومغناطیسی نیز از حاصل ضرب فرکانس در ثابت پلانک (h = 6.62 ͯ ۱۰-۳۴ ژول در ثانیه) به دست می آید. مقدار به دست آمده طبق این رابطه، میزان انرژی است که یک فوتون حمل می کند. علاوه بر ژول واحد دیگری که برای انرژی الکترومغناطیسی به کار برده می شود، الکترون ولت است.
رابطه بین انرژی با فرکانس

رفتار الکترون های اتم ها در مقابل تابش نور
با توجه به نظریه اتمی، الکترون ها در اوربیتال اتم ها و در پوسته های انرژی مشخصی در حال حرکت هستند. هر کدام از این لایه ها یا پوسته ها که با n خوانده می شوند، دارای مقدار مشخصی انرژی هستند. به دلیل امکان ناپذیر بودن قرار گرفتن الکترون ها بین پوسته ها، عدد n، صحیح و مثبت است. حال با تاباندن نور به یک اتم، الکترون های آن در ترازهای انرژی با دریافت انرژی می توانند به لایه های دیگر منتقل شوند. دریافت انرژی بیشتر، انتقال آن ها به لایه های دورتر را امکانپذیر می کند. برعکس با از دست دادن انرژی نیز این الکترون ها می توانند به لایه های پایین تر منتقل شوند. خطوط طیفی در نتیجه انتشار فوتون ها در طیف های خاصی توسط الکترون ها، به وجود می آید.
انواع طیف اتمی
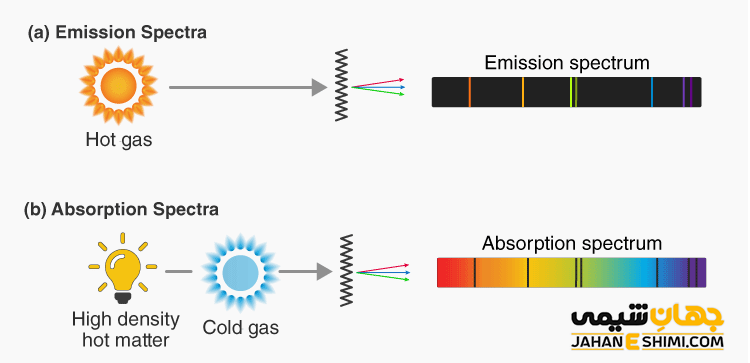
طیف نشری
وقتی به یک اتم انرژی داده می شود (مثلا با گرما دادن)، الکترون هایی که در ترازهای پایینی قرار دارند با گرفتن انرژی به ترازهای (لایه های) بالا منتقل می شوند. در این حالت گفته می شود، اتم برانگیخته شده است. حال این اتم برانگیخته برای این که به شکل پایدار خود در آید، تمایل به از دست دادن انرژی گرفته شده دارد. بنابراین با تابش این انرژی که برابر با اختلاف سطح انرژی دو تراز الکترونی هست، به حالت پایه بر می گردد.
فوتون هایی که در این اختلاف ترازهای انرژی تابش می شوند، مناسب با نوع اتم ها است. اتم های مختلف فوتون هایی با طول موج و فرکانس های خاص منتشر می کنند. به این فوتون ها، طول موج ها و فرکانس های منتشر شده طیف نشری می گویند. این طیف با انتقال الکترون های آن اتم از تراز الکترونی بالا به تراز الکترونی پایین، تشکیل می شود.
برای ایجاد یک طیف نشری، نور تولید شده از یک جسم را از یک منشور عبور می دهند.
طیف جذبی
فیزیکدان آلمانی به نام فرانهوفر کسی بود که در سال ۱۸۱۴ توانست خط های تاریکی را در طیف نور خورشید با نگاه دقیق در آن، کشف کند. در طیف پیوسته از نور خورشید خط های سیاه دیده می شود اما در برخی از این طول موج ها در نور رسیده از خورشید به زمین نیست. این موضوع به این دلیل اتفاق می افتد که برخی از گازهای موجود در اتمسفر خورشید، طول موج هایی را از نور خورشید جذب می کند. اما در طیف پیوسته ای که از نور خورشید تشکیل می شود، جای این طول موج ها به شکل خط های تاریک ظاهر می شود.
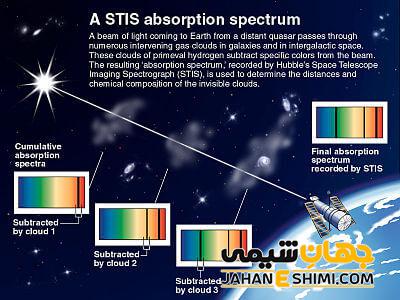
وقتی نور با تمام فرکانس ها و طول موج های مختلف به یک اتم تابانده می شود، توسط این اتم، فوتون هایی جذب می شود که انرژی برابر اختلاف سطح انرژی بین دو تراز در این اتم را دارد. با جذب این فوتون ها، الکترون در این اتم می تواند از تراز پایین به تراز بالا، منتقل شود. پس اگر نور خروجی آشکارسازی شود، فوتون هایی که دارای انرژی برابر با اختلاف انرژی دو تراز بودند، دیگر در این نور دیده نمی شود. به این فوتون ها، فرکانس ها و طول موج ها، طیف جذبی اتم مذکور گفته می شود.
اولین آزمایش جذب اتمی در قرن نوزدهم میلادی بود که نور سفید را از داخل بخار عنصر عبور دادند. پس از تشکیل طیف، دیده شد که خطوط تاریکی حاصل شده که نتیجه جذب توسط اتم های بخار است.
طیف اتمی پیوسته و گسسته
طیف اتمی را می توان در دو دسته پیوسته و گسسته دسته بندی کرد. در طیف پیوسته، تمام طول موج ها در آن در یک بازه مشخص بوده و هیچ فاصله ای بین این طول موج ها وجود ندارد. نمونه ای از این نوع طیف در نور خورشید دیده می شود.
طیف های گسسته که شامل طیف های نشری و جذبی اتم ها هستند، دارای یک سری طول موج های مشخصی هستند. بین این طول موج ها فاصله وجود دارد. خطوط طیفی در این نوع از طیف ها، نشان دهنده طول موج های خاص از یک اتم است. این خطوط طیفی سیاه یا روشن بوده و به شکل گسسته و جدا از هم قرار دارند.
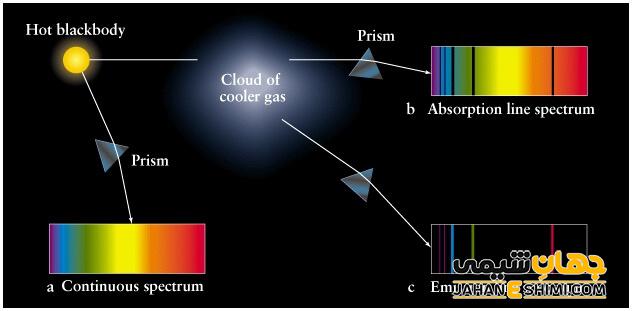
شکل طیف های نشری، خطوط طیفی روشن در زمینه سیاه هستند. در طیف های نشری، خطوط روشن همان فوتون هایی است که به وسیله اتم تولید شده است. اما شکل طیف های جذبی، زمینه روشنی است که خطوط طیفی سیاه در آن قرار دارند. در این طیف خط های سیاه، نشان دهنده فوتون هایی است که اتم جذب کرده است.
نکته
طیف های اتمی نشری و جذبی مکمل یکدیگر هستند. چون وقتی الکترونی در یک اتم از تراز A به تراز پایین تر B منتقل می شود و در طیف نشری مربوط به این اتم، یک خط روشن را در طول موج x ایجاد می کند، در طیف جذبی همان الکترون با انتقال از تراز B به تراز بالای A، خط سیاه و تاریکی را در همان طول موج ایجاد خواهد کرد.
کاربرد طیف اتمی
هر اتمی دارای سطوح انرژی مخصوص به خود است، به همین دلیل برای هر عنصر، طیف های نشری و جذبی ویژه ای وجود دارد. پس می توان گفت هر عنصری طیف اتمی منحصر به فرد خود را دارد. طیف اتمی مانند اثر انگشت برای هر اتمی می تواند برای شناسایی و تشخیص آن ها به کار رود. کشف برخی از اتم ها مانند هلیم، با بررسی طیف اتمی آن ها انجام شده است. برای تشخیص جنس اجرام آسمانی که در فواصل دور از ما قرار دارند، از طیف های اتمی استفاده می شود.
طیف اتمی هیدروژن
در پیشرفت فیزیک کوانتومی و رسیدن به ساختار اتم ها، مطالعه طیف نشری اتم هیدروژن بسیار موثر بوده است. یک سری از طیف اتمی هیدروژن به همه خط های طیفی گفته می شود که از ترازهای مختلف به یک تراز مقصد منتقل می شوند. هر کدام از این سری ها نیز به نام افراد کشف و مطالعه کننده آن خطوط طیفی، نام گذاری شده اند. سری های طیف نشری اتم هیدروژن شامل سری لیمان، بالمر، پاشن، براکت، فوند و هامفری است.
لیمان : در این سری خطوط طیفی در طیف نشری اتم هیدروژن، از ترازهای بالاتری که از تراز n = 1 قرار دارند به این تراز، انتقال الکترون دارند.
بالمر : در این سری انتقال الکترون از ترازهای بالاتر از n = 2 به این تراز اتفاق می افتد که این خطوط طیفی را در طیف نشری اتم هیدروژن نشان می دهد.
پاشن : خطوط طیفی که در طیف نشری اتم هیدروژن مربوط به انتقال الکترون از ترازهای بالاتر از n = 3 به این تراز هستند این سری را تشکیل می دهند.
براکت : در این سری انتقال الکترون از ترازهای بالاتر از n = 4 به این تراز انجام می شود و مجموعه این خطوط طیفی در طیف نشری اتم هیدروژن را نشان می دهد.
فوند : در نهایت مجموعه خطوط طیفی که مربرط به طیف نشری اتم هیدروژن بوده و انتقال الکترون از ترازهای بالاتر از n = 5 به این تراز انجام می شود، سری فوند را تشکیل می دهد.
سری هامفری : به مجموعه خطوط طیفی طیف نشری اتم هیدروژن که مربوط به انتقال الکترون از ترازهای بالاتر از n = 6 به این تراز است.



















