
در علم شیمی، ثابت یونش باز (Base Ionization Constant) یا همان ثابت تفکیک بازی (Base Dissociation Constant)، معیاری جهت تعیین و مقایسه قدرت باز ها در یک محلول می باشد. به بیان دیگر، ثابت تفکیک بازی همان ثابت تعادل واکنش های شیمیایی تفکیک بازی یا حلال کافت می باشد. در مباحث پیشین نشریه جهان شیمی فیزیک، مطالبی در خصوص باز و باز به ویژه باز و باز لوئیس و همچنین ثابت تفکیک بازی ارائه شده است. در این مقاله با مفهوم ثابت یونش باز ها آشنا خواهید شد. در ادامه با ما همراه باشید.
فهرست مطالب این مقاله
۱- باز چیست ؟ شیمی هشتم
۲- دسته بندی باز ها
۳- ثابت یونش باز
۴- رابطه ثابت یونش باز و pKb
۵- ثابت یونش یون هیدروکسید
۶- ثابت یونش باز های چند ظرفیتی
فهرست مطالب
باز چیست ؟ شیمی هشتم
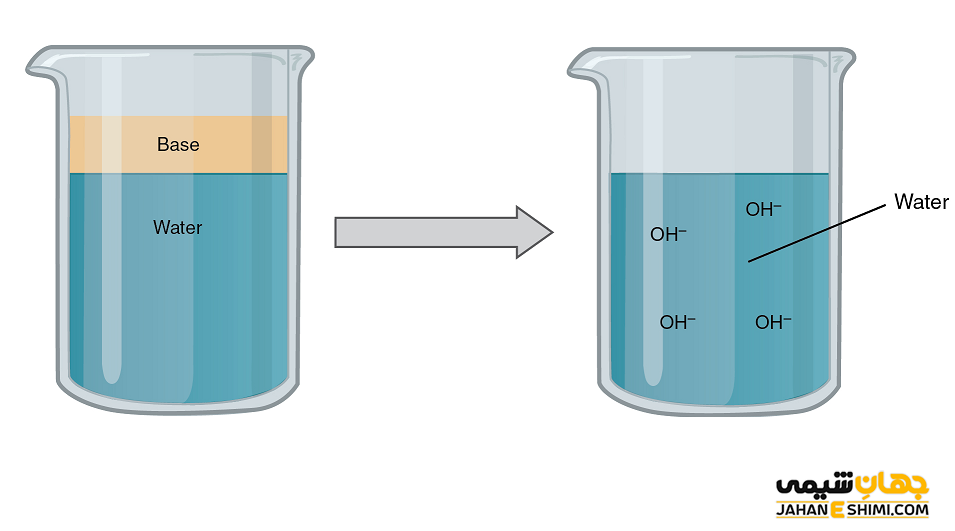
باز (Base) به مولکول یا یونی گفته می شود که قابلیت گرفتن یون هیدروژن (پروتون) و یا دادن جفت الکترون آزاد را داشته باشد. باز ها معمولا در اثر تفکیک در آب، یون های هیدروکسید (–OH) تولید می کنند. این ترکیبات در صورت تماس لغزنده بوده و تلخ مزه اند. بسیاری از پروتئین های بدن مانند هموگلوبین، از باز های مهم بدن محسوب می شوند. این ترکیبات زمانیکه با اسید ها واکنش دهند، نمک تشکیل می شود. لازم به ذکر است که هرچه غلظت یون های هیدروکسید آزاد شده بیشتر باشد، در نهایت محلول حاصله نیز خاصیت بازی بیشتری خواهد داشت. تا به امروز تعاریف مختلفی برای باز ها ذکر شده است.
این تعاریف عبارتند از :
- باز آرنیوس؛ باز آرنیوس به ماده شیمیایی گفته می شود که در اثر تفکیک در آب، یون های هیدروکسید (–OH) تولید کند. در واقع باز سبب افزایش غلظت یون های هیدروکسید در محلول آبی می گردد.
- باز برونستد-لوری؛ باز برونستد-لوری به ماده شیمیایی گفته می شود که قابلیت دریافت پروتون را داشته باشد. به عنوان مثال، یون بیکربنات (−HCO۳) می تواند یک پروتون گرفته و به H۲CO۳ تبدیل شود. توجه داشته باشید که بر خلاف تعریف آرنیوس، این تعریف را می توان در محیط های غیر آبی نیز استفاده کرد. در حقیقت می توان گفت که متداول ترین تعریفی که درباره باز ها کاربرد دارد، تعریف برونستد-لوری می باشد.
- باز لوییس؛ باز لوئیس به ماده شیمیایی گفته می شود که نوکلئوفیل است و قابلیت اهدای یک جفت الکترون را داشته باشد. در واقع، لوئیس به جای استفاده از انتقال پروتون، از انتقال الکترون بهره برده است. به بیان دیگر، باز ها مواد شیمیایی هستند که می توانند در واکنش های شیمیایی پیوند داتیو بدهند. بر اساس این تعریف، هر یک مولکول های CN−، CH۳COO– ، OH–، CO ، H۲O و NH۳ می توانند الکترون های ناپیوندی خود را در اختیار یک اسید لوئیس قرار دهند.
دسته بندی باز ها
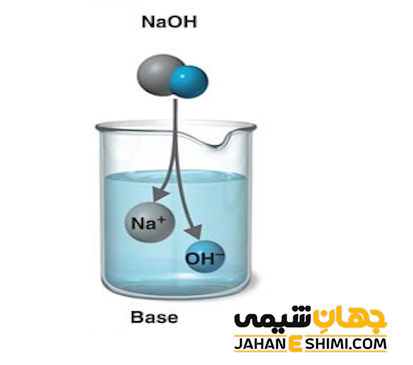
باز ها به طور کلی در دو دسته باز های قوی و ضعیف دسته بندی می شوند. قدرت یک باز در حقیقت به توانایی یا تمایل آن باز جهت دریافت یک پروتون اشاره می کند. در حقیقت باز ها نقطه مقابل اسید ها می باشند، زیرا یک اسید غلظت یون هیدرونیوم (+H3O) را در محلول آبی افزایش می دهد. در حالیکه یک باز غلظت این یون را کاهش خواهد داد. باز ها دارای قدرت های بازی متفاوتی نسبت به یکدیگر می باشند. باز قوی، به بازی گفته می شود که در اثر حل شدن در آب، به طور کامل یونیزه و تفکیک شود. این نوع از باز ها به طور کامل به یون های مثبت و منفی تفکیک می شوند. به عنوان مثال، به تفکیک باز قوی هیدروکسید سدیم توجه کنید :
NaOH (aq) → Na+ (aq) + OH− (aq)
در صورت تفکیک NaOH در آب، به طور کامل به یون های −OH و +Na تفکیک می شود، در نتیجه دیگر گونه NaOH (aq) در آب وجود نخواهد داشت. در این صورت، +Na به عنوان اسيد مزدوج باز قوي NaOH در آب، هیچ گونه خصلت اسيدي ندارد، پس تفكيك اسيدی آن و يا گرفتن آنیون OH که منجر به تولید دوباره NaOH شود، بی معنا خواهد بود.
نکته
به طور مشابه، باز ضعیف به بازی گفته می شود که به طور جزئی در آب یونیزه شده باشد. به عبارت دیگر می توان گفت که پروتون دهی یک باز ضعیف در آب به شکل نا تمام صورت می گیرد. به عنوان مثال، تفکیک باز ضعیف آمونیاک را در زیر می بینید.
NH۳ (aq) + H۲O (l) ⇋ NH۴+ (aq) + OH− (aq)
این باز در آب به طور کامل تفکیک نمی شود، بنابراین گونه NH۳ (aq) در آب به شکل دست نخورده یا تفکیک نشده نیز وجود دارد. علاوه بر آن، آنیون −OH در آب دارای خصلت بازی می باشد. این آنیون از طریق هيدروليز بازي يا گرفتن پروتون می تواند باعث تولید H۲O (aq) شود.
ثابت یونش باز
دقت داشته باشید که برای مقایسه قدرت بازی، معیاری به نام ثابت یونش بازی (Kb) وجود دارد. در واقع به واکنش گرفتن پروتون از مولکول های حلال، واکنش تفکیک بازی یا حلال کافت گفته می شود. از این رو، واکنش تفکیک بازی و ثابت تعادل مربوط به آن (ثابت تعادل تفکیک بازی یا ثابت تعادل حلالکافت)، در حالت کلی به شکل زیر می باشد :
A− (sol) + HS (l) ⇋ HA (sol) + S− (sol)
Kb =[ HA][S −] / [A−]
لازم به ذکر است که افزایش مقدار Kb در حقیقت بیانگر افزایش مقدار تفکیک باز و در نتیجه افزایش قدرت بازی می باشد. حال اگر حلال آب باشد، در این صورت این واکنش تفکیک را می توان واکنش هیدرولیز بازی نامید. در نتیجه خواهید داشت :
A− (sol) + H۲O (l) ⇋ HA (aq) + OH− (aq)
Kb = [HA][OH−] / [H۲O][A−]
همانطور که می دانید، غلظت آب خالص در همه واکنش های محلول در آب، مقداری ثابتی است. از این رو، معادله ثابت تعادل به شکل زیر خواهد بود که در آن، Kb ثابت تفکیک باز یا ثابت یونش باز می باشد.

جالب است بدانید که
ثابت یونش باز یا ثابت تفکیک باز در واقع همان ثابت تعادل واکنش باز (B) و آب می باشد. در حالت کلی، واکنش تفکیک بازی و ثابت تعادل مربوطه به صورت زیر می باشد :
B (aq) + H۲O (l) ⇋ BH+ (aq) + OH− (aq)
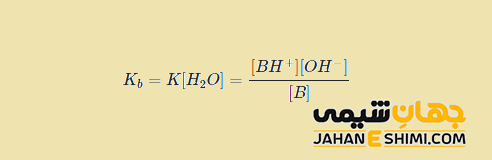
توجه داشته باشید که در معادله فوق، واحد [B]، [−OH] و [+BH] بر حسب مول بر لیتر می باشد. علاوه بر آن، با توجه به دو معادله K و Kb مشخص می شود که مقدار عددی این دو ثابت تعادل به میزان غلظت آب (یعنی ۵۵/۳ مولار) با یکدیگر تفاوت دارند. مقدار ثابت یونش بازی در دمای معین، عددی ثابت می باشد. افزایش مقدار آن در حقیقت بیانگر افزایش قدرت بازی و همچنین نشان دهنده افزایش مقدار تفکیک باز می باشد.
رابطه ثابت یونش باز و pKb
مقادیر Kb برای بیشتر باز ها، بسیار کوچک و یا حتی بسیار بزرگ می باشد، بنابراین مفهوم و مقایسه این اعداد کمی سخت است. از طرفی دیگر، جهت محاسبات قدرت بازی و بدست آوردن ثابت تفکیک بازی می توان به جای نوشتن عبارات توان دار از لگاریتم منفی استفاده کرد. پس از معیار دیگری به نام pKb بهره می برند. فرمول محاسبه pKb به صورت زیر می باشد :
pKb = -log Kb
Kb = 10−pKb
توجه داشته باشید که در محاسبات pKb از لگاریتم منفی استفاده می شود، از این رو، مقادیر عددی کم pKb نشان دهنده ثابت تفکیک بازی بزرگتر و در نتیجه، قدرت بازی بالاتر می باشد. به عنوان مثال، مقادیر عددی pKb و مقایسه قدرت بازی چند باز در جدول زیر آورده شده است. همان گونه که مشاهده می کنید، از بالا به پایین جدول، قدرت بازی کاهش پیدا کرده است. لازم به ذکر است که Kb و pKb بدون واحد می باشند.
| فرمول شیمیایی | pKb |
| −F | ۱۰.۸ |
| KCOOH | ۱۰.۲۵ |
| NaClO | ۶.۴۸ |
| NH۳ | ۴.۷۵ |
| NH۴OH | ۴.۷۵ |
| CH۵N | ۳.۳۶ |
ثابت یونش یون هیدروکسید
با توجه به معادله یونش یون هیدروکسید، مشخص می شود که مقادیر Kb و pKb بر طبق واکنش زیر بدست می آید.
H۲O (l) + OH− (aq) ⇌ OH− (aq) + H۲O (l)
Kb = [OH−] / [OH−] = 1
pKb = -log 1 = 0
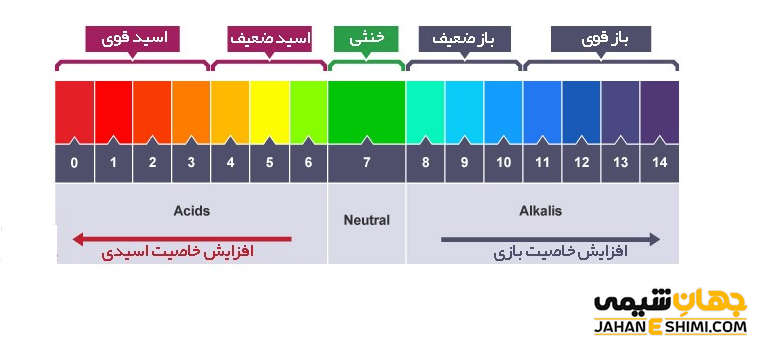
بنابراین با توجه به معادله مشخص می شود که مقادیر Kb و pKb یون هیدروکسید به ترتیب برابر با ۱ و صفر می باشد. از این رو، یون هیدروکسید در مرز میان باز های قوی و باز های ضعیف قرار می گیرد. در واقع اگر بازی Kb بزرگتر از یک و یا اینکه PKb کوچکتر از صفر داشته باشد، بازی قوی خواهد بود. در حالیکه اگر Kb بازی کوچکتر از یک و یا PKb آن بزرگتر از صفر باشد، در این صورت باز ضعیف محسوب می شود. به عنوان مثال مقایسه قدرت بازی بازهای مختلف به صورت زیر می باشد :
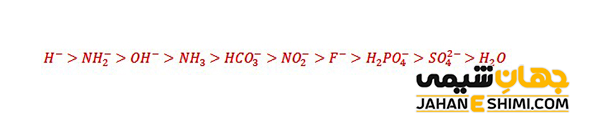
لازم به ذکر است که در محلول های آبی، باز های قوی به طور کامل تفکیک می شوند، پس در نهایت آنها تبدیل به یون هیدروکسید می شوند. در این صورت دیگر در محلول آبی یونی وجود نخواهند داشت، در نتیجه قوی ترین باز موجود در محلول آبی همان یون هیدروکسید خواهد بود. پس می توان قدرت تمام آنها را در محلول های آبی یکسان با یون هیدروکسید در نظر گرفت (در واقع، آب برای بازهای قوی اثر هم تراز کنندگی دارد). به این دلیل، مقایسه قدرت باز های قوی در محیط های آبی ممکن نمی باشد.
جالب است بدانید که
قدرت بازی در هیدروکسید های فلزی وابسته به شعاع کاتیون آن هیدروکسید می باشد، شعاع کاتیون در واقع بر روی میزان جاذبه آنها جهت نگه داشتن OH− تاثیر دارد. دقت داشته باشید که هر چه شبکه بلوری ماده شیمیایی مورد نظر، راحت تر در آب متلاشی گردد، می تواند راحت تر آنیون OH را آزاد کند، پس قدرت بازی بیش تری نیز خواهد داشت. به عبارتی دیگر، هر چه شعاع کاتیون مورد نظر بزرگتر باشد، تراکم بار سطحی بر روی آن کمتر بوده، در نتیجه جاذبه کاتیون با آنیون OH نیز کمتر می شود. در این صورت قدرت بازی بیشتر خواهد شد. در نتیجه می توان گفت که :
- قدرت بازی در هیدروکسید های فلزات قلیایی و قلیایی خاکی جدول تناوبی، از سمت بالا به پایین افزایش پیدا می کند.
- قدرت بازی هیدروکسید های گروه فلزات قلیایی بیشتر از گروه فلزات قلیایی خاکی می باشد.

ثابت یونش باز های چند ظرفيتی
باز ها همانند اسید ها مي توانند تك ظرفيتی يا چند ظرفيتی باشند. باز چند ظرفيتی به ترکیبی گفته می شود که بتواند بیش از یک هیدروژن بگیرد. این باز می تواند به طور متوالی تفکیک شود. در حالیکه باز های تک ظرفيتی فقط یک واکنش تفکیک بازی دارند، در نتیجه فقط یک ثابت یونش بازی نیز خواهند داشت. به عبارت دیگر، يك باز با ظرفيت n، توانايی و قابلیت دریافت حداکثر n پروتون را دارد. از جمله باز های چند ظرفيتی می توان به یون فسفات (۳–PO4) اشاره کرد. این باز حداکثر می تواند سه پروتون بگیرد، بنابراین یک باز سه ظرفیتی می باشد. به عبارت دیگر، به تعداد ظرفیت یک باز می توان ثابت تفکیک بازی (یا ثابت حلالکافت) در نظر گرفت که در واقع با شماره از یکدیگر متمایز می شوند.
به عنوان مثال، همان باز سه ظرفيتی PO۴-۳ را در نظر بگیرید. این باز بسته به مقدار pH محلول می تواند یک، دو یا سه واکنش تکفکیک بازی داشته باشد. توجه داشته باشید که هر واکنش به طور جداگانه یک ثابت یونش باز دارد، (Kb1، Kb2 و Kb3).
PO۴-۳ (aq) + H۲O (l) ⇌ HPO۴-۲ (aq) + OH− (aq) Kb1
HPO۴-۲ (aq) + H۲O (l) ⇌ H۲PO۴– (aq) + OH− (aq) Kb2
H۲PO۴– (aq) + H۲O (l) ⇌ H۳PO۴ (aq) + OH− (aq) Kb3
توجه داشته باشید که در این گونه باز ها، Kb1 بیشتر از Kb2 و همچنین Kb2 هم بیشتر از Kb3 می باشد. در باز های چند ظرفيتی، با دریافت پروتون از مولکول آب، بار منفي باز کاهش می يابد، پس تمايل آن مولکول برای گرفتن پروتون نیز كاهش پیدا می کند. از این رو، ثابت تعادل بازی هم کم می شود. بنابراین براي باز هاي چند ظرفيتی داریم :




















