فلزات واسطه خارجی – عناصر دسته d جدول تناوبی
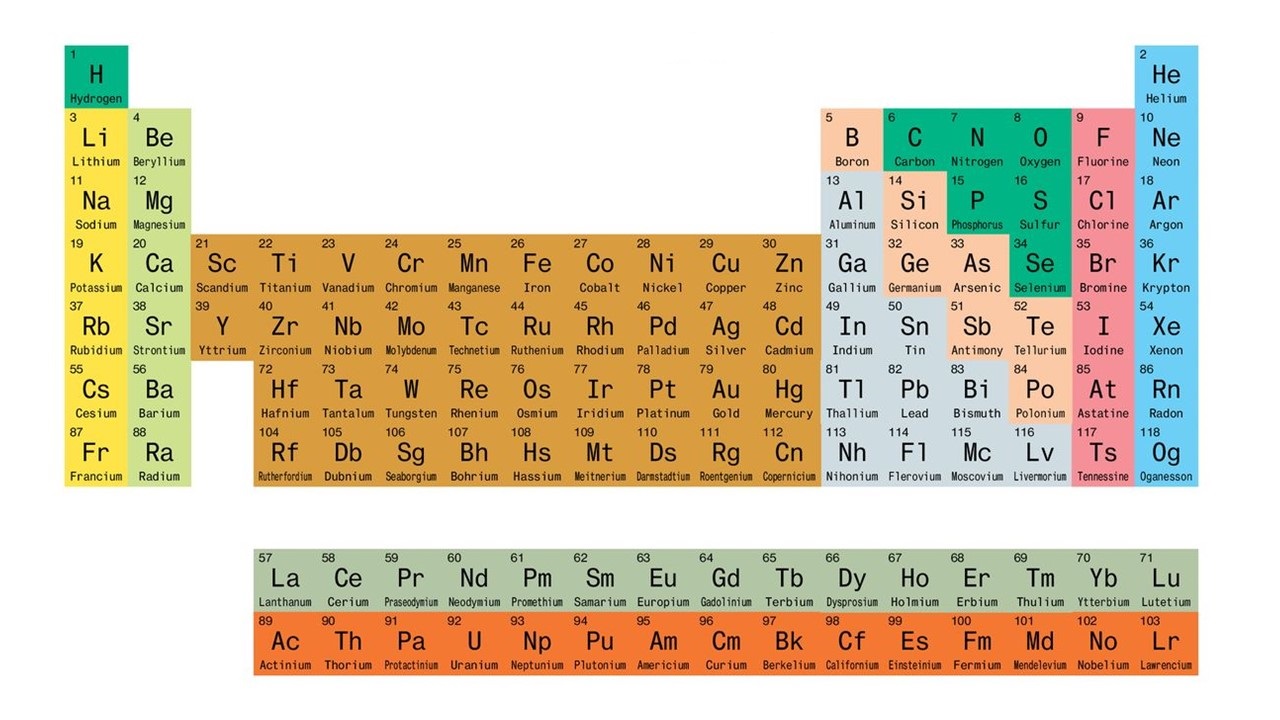
فلزات واسطه خارجی در جدول تناوبی عناصری هستند که گروه ۳ تا ۱۲ جدول را اشغال می کنند. در این عناصر اوربیتال d در حال پر شدن از الکترون است.

چارلز باری شیمی دان انگلیسی اولین کسی بود که نام واسطه را برای این عناصر به کار برد. این مقاله نشریه جهان شیمی فیزیک به بررسی خواص و کاربردهای این عناصر مهم می پردازد.
فهرست مطالب
خواص کلی عناصر واسطه خارجی
همه عناصر واسطه خاصیت فلزی دارند. از نظر موقعیت در جدول تناوبی از دوره چهارم شروع می شوند و بین فلزات قلیایی خاکی و گروه بور قرار گرفتند. نکته ای که در آرایش الکترونی آن ها وجود دارد در لایه ظرفیت آن ها سطح انرژی تراز (n-1)d پایین تر از سطح انرژی تراز ns است. در فلزات واسطه ردیف چهارم اوربیتال 3d، ردیف پنجم اوربیتال 4d، ردیف ششم اوربیتال 5d و ردیف هفتم اوربیتال 6d در حال پرشدن است.

توجه
آرایش الکترونی اولین عنصر گروه ۳ به شکل زیر است :
[Ar]4s۲3d۱
استثنا
در ردیف چهارم آرایش الکترونی مس با این روند پرشدن تفاوت دارد (3d۱۰4s۱) و این به خاطر پایداری بیشتر در این شکل آرایشی است. آرایش الکترونی کروم نیز حالت استثنا (d۵s۱) دارد. در بین این عناصر روی، کادمیم و جیوه چون آرایش لایه ظرفیت آن ها (d۱۰s۲) مانند آرایش الکترونی گاز نجیب اوکتت است به آن ها فلزات پس واسطه می گویند.
الکترونگاتیوی
در عناصر واسطه چون اندازه اتم کوچک بوده و بار موثر هسته آن زیاد است در مقایسه با عناصر گروه های اصلی جدول تناوبی الکترونگاتیوی و انرژی یونش بالاتری دارند.
خواص فیزیکی فلزات واسطه خارجی
فلزات واسطه خارجی به جز روی، کادمیم و جیوه چگالی، نقاط ذوب و جوش و سختی زیادی دارند. چون در این فلزات الکترون های اوربیتال d در پیوند فلزی شرکت کرده و بین مولکول ها تعداد الکترون های اشتراکی زیاد شده و انرژی بستگی بلورها زیاد می شود. اما در فلزات گروه ۱۲ چون اوربیتال d پرشده دارند نقطه ذوب و جوش آن ها پایین است. در بین این فلزات واسطه جیوه به شکل مایع و بقیه جامد می باشند. فلزات واسطه خارجی رسانای خوب جریان الکتریکی می باشند. پس نتیجه می شود خواص فلزی فلزات واسطه به الکترون های نامستقر آن ها در لایه ظرفیت مربوط می باشد.

توجه
فلزات واسطه خارجی قابلیت شکل پذیری، ورقه و مفتول شدن دارند، چکش خوارند، خاصیت انعطاف پذیری دارند، به جز جیوه، روی و کروم در مقابل ضربه و فشار مقاوم هستند.
چون در فلزات واسطه خارجی الکترون ها به تراز ماقبل آخر اضافه می شود دافعه بین این الکترون ها با الکترون های تراز آخر زیاد شده، از تغییرات زیاد خواص عناصر این دسته جلوگیری می کند. به همین جهت خصوصیات این دسته از عناصر در یک دوره مثل شعاع اتمی تغییرات بسیار کمی نشان می دهد.
عدد اکسایش
از خصوصیات فلزات واسطه خارجی می توان به عددهای اکسایش مختلف آن اشاره کرد. مثلا وانادیم عدد اکسایشش بین ۱- تا ۵+ است. بالاترین عدد اکسایش عناصر ردیف اول فلزات واسطه خارجی با تعداد الکترون های ظرفیت آن ها برابر است. عدد اکسایش منگنز دراین ردیف ۷+ است. روتینیوم با عدد اکسایش ۷+ و ایریدیم با عدد اکسایش ۹+ بیشترین عددهای اکسایش را در ردیف دوم و سوم دارا هستند.
ترکیبات رنگی
فلزات واسطه خارجی تشکیل ترکیبات و کمپلکس های رنگی می دهند. تشکیل کمپلکس به احاطه شده یون عنصر واسطه توسط یون ها و مولکول های قطبی گفته می شود. این کمپلکس ها نسبت به فلزات قلیایی خاکی سختی بیشتر و واکنش پذیری کمتری دارند. علت رنگی بودن در فلزات واسطه انتقال بار است. در حضور لیگاندهای دیگر اوربیتال های d دارای انرژی های مختلفی می شوند. الکترون ها می توانند با جذب فوتون از اوربیتال های با انرژی کمتر به اوربیتال های با سطح انرژی بیشتر منتقل می شوند. انتقال بار یا از یک اوربیتال لیگاند به یک اوربیتال فلزی انجام می شود و یا جهش بار (انتقال الکترون) را از یک اوربیتال d به اوربیتال d دیگر داریم. همین جهش های الکترونی علت رنگی شدن این ترکیبات است. ترکیبات این فلزها در حالت اول نسبت به انتقال بار اوربیتال های d پررنگ تر هستند. یک مثال از این ترکیبات یدید جیوه قرمز می باشد.

خواص مغناطیسی فلزات واسطه خارجی
خاصیت مغناطیسی در این ترکیبات با داشتن تک الکترون در اوربیتال آن ها در حالت آزاد یا در حالت اکسایشی تعریف می شود. اگر هر اسپین در اوربیتال به عنوان یک آن ربا فرض شود دو الکترون در جهت مخالف هم اثر مغناطیسی یکدیگر را خنثی می کنند. بسیاری ترکیبات فلزات واسطه مانند آهن، کبالت، نیکل و غیره با داشتن الکترون جفت نشده پارامغناطیس هستند. اما روی و کادمیم در این عنصرها در حالت آزاد دارای اوربیتال های با جفت الکترون هستند و پوسته الکترونی پر دارند خاصیت دیا مغناطیسی دارند. بعضر از این عنصرها مانند کروم هم با اینکه الکترون جفنت نشده دارند آنتی فرومغناطیس هستند.

رسانایی گرمایی در فلزات واسطه خارجی
فلزات واسطه رسانای خوبی برای گرما و برق هستند. هرچه رسانایی گرمایی بالایی داشته باشند، رسانایی الکتریکی زیادی هم خواهند داشت. در بین این فلزات عناصر گروه IB به دلیل داشتن اوربیتال های تراز d پر و داشتن یک الکترون در اوربیتال S قدرت رسانایی بالایی دارند.
خواص کاتالیزوری
فلزات واسطه چون اعداد اکسایش مختلف داشته و می توانند کمپلکس تشکیل دهند به عنوان کاتالیزور استفاده می شوند. در کاتالیزورهای جامد روند انجام واکنش شامل افزایش غلظت واکنش دهنده ها با تشکیل پیوند بین مولکول های واکنش دهنده و اتم ها در سطح کاتالیزور است. یکی از فرآیندهای کاتالیستی فلزات واسطه واکنش خود کاتالیزوری است که در آن سرعت واکنش توسط فرآورده های واکنش زیاد می شود.
کاربردهای فلزات واسطه خارجی
یکی از کاربردهای این فلزات ساخت آلیاژهاست که اوربیتال های تک الکترونی در اتم یک فلز با الکترون های تک اوربیتال های عناصر دیگر ترکیب شده و آلیاژها را می سازند. به دلیل خواص منحصربه فردی که این عناصر دارند از آن ها از ساخت میخ های آهنی گرفته تا ساخت فضاپیما استفاده می شود. در اینجا کاربرد برخی فلزات واسطه را به اختصار بیان می کنیم.
کاربرد آهن
آهن فراوان ترین فلز واسطه در دنیاست. از آهن در تهیه آلیاژهای فولاد، در تولید ابزارها، وسایل ساختمانی، رنگ ها، کودها، وسایل آرایشی، به عنوان کاتالیزور در تولید آمونیاک و وسایل نقلیه استفاده می شود. همان طور که می دانیم نقش مهم آهن در زندگی موجودات، ایجاد هموگلوبین برای حمل اکسیژن در خون بسیار حائز اهمیت است.
کاربرد روی
روی فلزی نرم وسفید با رنگ خاکستری متمایل به آبی است که در آب حل نمی شود اما در اسیدها و بازها قابل حل است. از روی بیشتربرای آبکاری الکتریکی فلزات استفاده می شود. از کاربردهای دیگر روی استفاده در صنعت خودروسازی، ریخته گری، تولید آلیاژ برنج، تولید ظروف، کشتی سازی و تولید باتری هایی که از باتری های لیتیمی قدرتمندتر است را می توان نام برد.

کاربرد کروم
کروم فلزی براق به رنگ خاکستری و سخت است که چون قابلیت جلاپذیری دارد و به راحتی تیره نمی شود مصرف بالایی دارد. روی کاربردهایی چون آب کاری، ساخت آلیاژ، ترکیب پتاسیم آن در تمیز کردن ظروف آزمایشگاه، ساخت قالب های پخت آجر و به صورت دندانه در رنگرزی را دارد.
کاربرد مس و طلا
مس فلزی بسیار مهم در ساخت سیم های الکتریکی است. همچنین در ساخت سکه های ارز، ساخت آلیاژ برنج و برنز، لوله های آب، بخاری، ظروف مسی و سیستم های خنک کننده از مس استفاده می شود. طلا فلزی بسیار گران قیمت است که رسانای خوب الکتریسیته بوده ودر مقابل هوا و آب دچار خوردگی نمی شود. کاربرد زیاد آن در ساخت جواهرات است.
نافلز های جدول تناوبی
عناصر را می توان به عنوان فلز، نافلز یا متالوئید طبقه بندی کرد. فلزات رسانای خوبی برای گرما و الکتریسیته هستند و چکش خوار و انعطافپذیر هستند. اکثر فلزات در دمای اتاق جامد هستند. بسیاری از نافلزات عنصری در دمای اتاق گاز هستند، در حالی که برخی دیگر مایع و جامد هستند. متالوئیدها از نظر خواص متوسط هستند. آنها از نظر خواص فیزیکی بیشتر شبیه نافلزات هستند، اما تحت شرایط خاص، می توان چندین مورد از آنها را برای رسانای الکتریسیته ساخت. این نیمه هادی ها در رایانه ها و سایر وسایل الکترونیکی ضروری هستند.
در بسیاری از جداول تناوبی، یک خط مشکی ناهموار در امتداد سمت راست جدول، فلزات را از نافلزات جدا می کند. فلزات در سمت چپ خط قرار دارند (به جز هیدروژن که یک نافلز است)، نافلزات در سمت راست قرار دارند و عناصر بلافاصله در مجاورت خط متالوئیدها هستند. لیست نافلزهای موجود در جدول تناوبی عناصر را می توان در گوشه سمت راست بالای جدول تناوبی یافت. اینها شامل گروه غیر فلزی، گازهای نجیب و هالوژن ها می شود.
در مقایسه با عناصری که در فهرست فلزات جدول تناوبی عناصر یافت می شوند، غیرفلزها کدر یا براق نیستند. آنها رسانای ضعیف گرما و الکتریسیته هستند اگرچه انرژی یونیزاسیون و الکترونگاتیوی بالایی دارند. عناصر غیرفلزی موجود در جدول، چکش خوار یا شکل پذیر نیستند و معمولاً شکننده بوده و چگالی کمتری دارند. آنها همچنین دارای نقطه ذوب پایین تر و همچنین نقطه جوش هستند و حالت اکسیداسیون منفی دارند بنابراین در واکنش ها الکترون به دست می آورند.
فهرست نافلزات جدول تناوبی عناصر معمولاً در حالت جامد رنگارنگ هستند. آنها کاربردهای جهانی دارند، مانند مواد ضروری زندگی از جمله اکسیژن، هیدروژن و کربن که در کودها، در مبردها و در داروسازی مورد استفاده قرار می گیرند. آنها را می توانید در بسیاری از صنایع مشاهده کنید. در واقع کاربردهای عناصر غیرفلزی کمتر از فلزات نیست. برخی از آنها کاملا شناخته شده هستند در حالیکه برخی دیگر ممکن است خیلی در کاربردهای امروزی شناخته شده نباشند.
عناصر واسطه در شیمی دهم
عناصر واسطه به گروهی از عناصر فلزی گفته می شود که در جدول تناوبی بین عناصر گروه های اصلی قرار دارند. این عناصر بیشتر در بلوک d قرار می گیرند و ویژگی های خاصی دارند که باعث تمایز آنها از دیگر فلزات می شود. برخی از این فلزات شامل آهن، مس، نیکل، کبالت و غیره هستند که کاربردهای گستردهای در صنعت و علوم مختلف دارند.
یکی از ویژگیهای بارز عناصر واسطه، داشتن اوربیتالهای d نیمه پر یا پر است که باعث می شود که این عناصر قابلیت تشکیل ترکیبات مختلف با حالات اکسیداسیون متنوع را داشته باشند. به همین دلیل این عناصر در واکنشهای شیمیایی بسیار فعال هستند و با عناصر دیگر پیوندهای متفاوتی تشکیل می دهند.
عناصر واسطه همچنین دارای رنگ های مشخص و زیبایی در ترکیبات خود هستند. این رنگها به دلیل انتقال الکترون ها در اوربیتالهای d و اثرات میدان کریستالی به وجود می آیند. این عناصر همچنین دارای خواص مغناطیسی خاصی هستند که به ساختار الکترونی آنها وابسته است. مثلا آهن و کبالت خاصیت آهنربایی دارند که در فناوریهای مختلف کاربرد دارد.
از نظر کاربرد، عناصر واسطه نقش مهمی در صنعت ایفا میکنند. مثلا آهن در تولید فولاد، مس در صنعت برق، نیکل در ساخت آلیاژها و کبالت در باتری های قابل شارژ استفاده می شود. علاوه بر این به عنوان کاتالیزور در واکنش های شیمیایی عمل کرده و سرعت واکنش ها را افزایش می دهند. شناخت ویژگیها و کاربردهای عناصر واسطه اهمیت زیادی در علوم پایه دارد و در شیمی دهم بطور مفصل در رابطه با آنها شرح داده شده است.



















