لیگاند و انواع آن چیست؟ – فرق لیگاند با رسپتور

به ذره ای که می تواند یون و یا مولکول باشد و برای تشکیل یک کمپلکس کوئوردیناسی، یک جفت الکترون به اتم و یا یون فلز مرکزی اعطا کند، به نام لیگاند خوانده می شود. دانش هایی که در آن ها، لیگاند و انواع آن اهمیت بسیاری دارد، شیمی معدنی زیستی و شیمی دارویی، شیمی محیط زیست و کاتالیز همگن است. این مقاله نشریه جهان شیمی فیزیک ما را با تعریف لیگاند و انواع آن آشنا می کند.
لیگاند
مولکول ها و یا یون های خنثی که وقتی با دادن جفت الکترون، با اتم فلز مرکزی پیوند برقرار می کنند و تشکیل کمپلکس های کوئوردیناسی می دهند، لیگاند نامیده می شوند. چون لیگاندها در برقراری این پیوندها در نقش دهنده جفت الکترون هستند، به عنوان باز لوئیس عمل کرده ولی فلز مرکزی به عنوان پذیرنده الکترون در نقش اسید لوئیس عمل می کند. در برخی از موارد استثنا می توان نقش اسید لوئیس را از لیگاندها مشاهده کرد.
برای اولین بار کلمه لیگاند توسط آلفرد استاک شیمیدان آلمانی به کار برده شد که این کلمه از واژه ی لاتین Ligare گرفته شده است. معنای این کلمه اتصال، گره زدن و یا بستن است. حداقل یک اتم یا یک جفت الکترون باید در یک لیگاند باشد تا بتواند با اتم مرکزی پیوند برقرار کند. پیوندی که بین لیگاند و اتم مرکزی ایجاد می شود از نوع کووالانسی است. در تشکیل کمپلکس های کوئوردیناسی، فلزات و شبه فلزات در هر شرایطی شرکت کرده و واکنش پذیری اتم مرکزی به وسیله لیگاندها تعیین می شود.
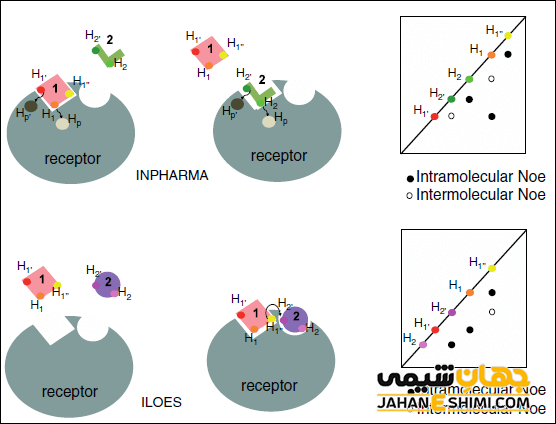
لیگاندها می تواند یک نوع کاتیون باشد مانند NO+ و N۲H۵+، یا یک آنیون باشد مانند OH– و هالیدها و یا یک لیگاند خنثی مانند CO و NO باشد.
انواع لیگاندها
دسته بندی لیگاندها با روش های مختلفی چون پیوند با اتم مرکزی، بار، اندازه و تعداد الکترون های اهدایی انجام می گیرد که بر این اساس، انواع لیگاندها را بر اساس پیوندپوشی و دندانگی تقسیم می کنند. بر این اساس با توجه به این که چه تعداد الکترون بین لیگاند و اتم مرکزی قرار می گیرد، لیگاندها به دو دسته ی لیگاندهای L و X تقسیم می شود.
لیگاندهای L
در این نوع لیگاندها، دو الکترون به اشتراک گذاشته شده بین لیگاندها و اتم مرکزی از جفت الکترون های غیرپیوندی بوده و نوع پیوند ایجاد شده نیز از نوع داتیو است.
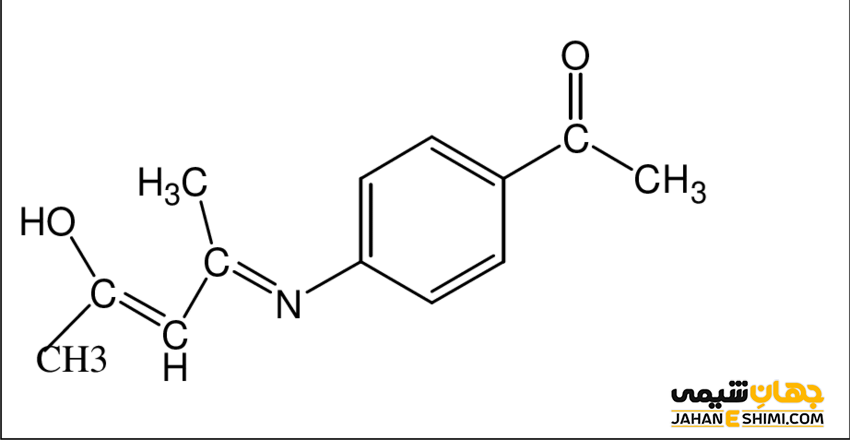
لیگاندهای X
این نوع لیگاندها یک الکترون از خود با یک الکترون از اتم مرکزی به اشتراک گذاشته و نوع پیوند ایجاد شده نیز از نوع کووالانسی خواهد بود.
لیگاند یک دندانه
به لیگاندهایی که با اتم مرکزی تنها یک پیوند ایجاد می کند، لیگاندهای تک دندانه گفته می شود که به نام یک دندان نیز خوانده می شوند. از انواع لیگاندهای تک دندانه می توان انواع هالیدها، آکوا، یون هیدروکسید، کربن مونوکسید، یون سیانید و یون تیوسیانات را نام برد.
لیگاندهای دو دندانه
به لیگاندهایی که باز لوئیس بوده و دو جفت الکترون به اتم مرکزی می دهد، لیگاندهای دو دندانه و یا شلات کننده می گویند. از مهمترین لیگاندهای دو دندانه، اتیلن دی آمین و یون اگزالات هستند. لیگاند دو دندانه اتیلین دی آمین، وقتی کمپلکس کوئوردیناسی با یون فلزی تشکیل می دهد در ساختار آن یک حلقه پنج عضوی تشکیل می دهد. اتم های نیتروژن در این لیگاند با آزاد کردن دو الکترون می تواند پیوند با اتم یا یون مرکزی در ساختار کمپلکس ایجاد کند. از لیگاندهای دو دندانه دیگر می توان به فنانترولین و یون استیل استونات فنانترولین اشاره کرد.
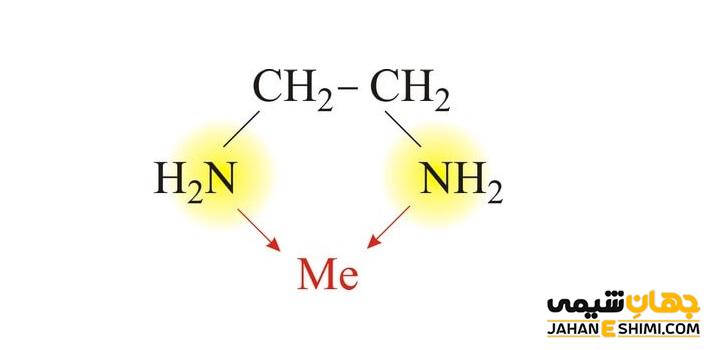
لیگاندهای سه دندانه
نوعی از لیگاندها که می تواند با اتم یا یون مرکزی سه پیوند در نتیجه ی اهدای سه جفت الکترون ایجاد کند، لیگاند سه دندانه گفته می شود. از جمله این لیگانده می توان به TACN اشاره کرد.
لیگاندهای چند دندانه
نوع دیگری از لیگاندها که به لیگاندهای چند دندانه معروف هستند، تعداد جفت الکترون هایی که به اتم یا یون مرکزی اهدا می کنند، دو یا بیشتر بوده و به تعداد این جفت الکترون ها، پیوند برقرار می شود. این لیگاندها می تواند چهار دندانه، پنج دندانه و یا شش دندانه باشد.
عامل کی لیت کننده
به لیگاندهای دو دندانه و چند دندانه ای که می تواند مانند یک چنگالی، اتم یا یون مرکزی را در احاطه خود در آورد، عامل کی لیت کننده گفته می شود. به این نوع لیگاندها، کلات کننده، کلاته کننده و کلیت ساز نیز می گویند. معمول ترین عامل کی لیت کننده، یون اتیلن دی آمین تترااستات است که می تواند در تشکیل یون کمپلکس پایدار با اتم سرب شرکت کند. از این خاصیت این لیگاند برای درمان مسمومیت استفاده می شود، زیرا با تشکیل چنین کمپلکسی باعث جداسازی عنصر سرب از خون و بافت های بدن می شود. برای پاک کردن نشتی حاصل از فلزات رادیواکتیو نیز از این نوع لیگاندها استفاده می شود.
اثر کی لیت
لیگاندهای کی لیت ساز می توانند به یون و یا اتم مرکزی متصل شوند که به میزان تمایل آن ها به چنین اثری در مقایسه با لیگاندهای تک دندانه غیر کی لیت ساز، اثر کی لیت گفته می شود.
لیگاند آمبیدنتات
به لیگاندهایی که در ساختار خود بیش از یک اتم داشته و توانایی اهدا کردن الکترون دارند، لیگاند آمبیدنتات می گویند. نمونه ای از این نوع لیگانده، یون تیوسیانات است که اتم های گوگرد و نیتروژن موجود در ساختار آن می تواند در تشکیل پیوند با اتم و یا یون فلز مرکزی شرکت کند.
لیگاند پل ساز
نوعی از لیگااندها که توانایی تشکیل پیوند با بیشتر از یک اتم و یا یون فلزی دارد، لیگاندهای پل ساز گفته می شود. یون هیدروکسید، کربونیل، آمینو، هیدرید و اکسید نمونه هایی از لیگاندهای پل ساز هستند.
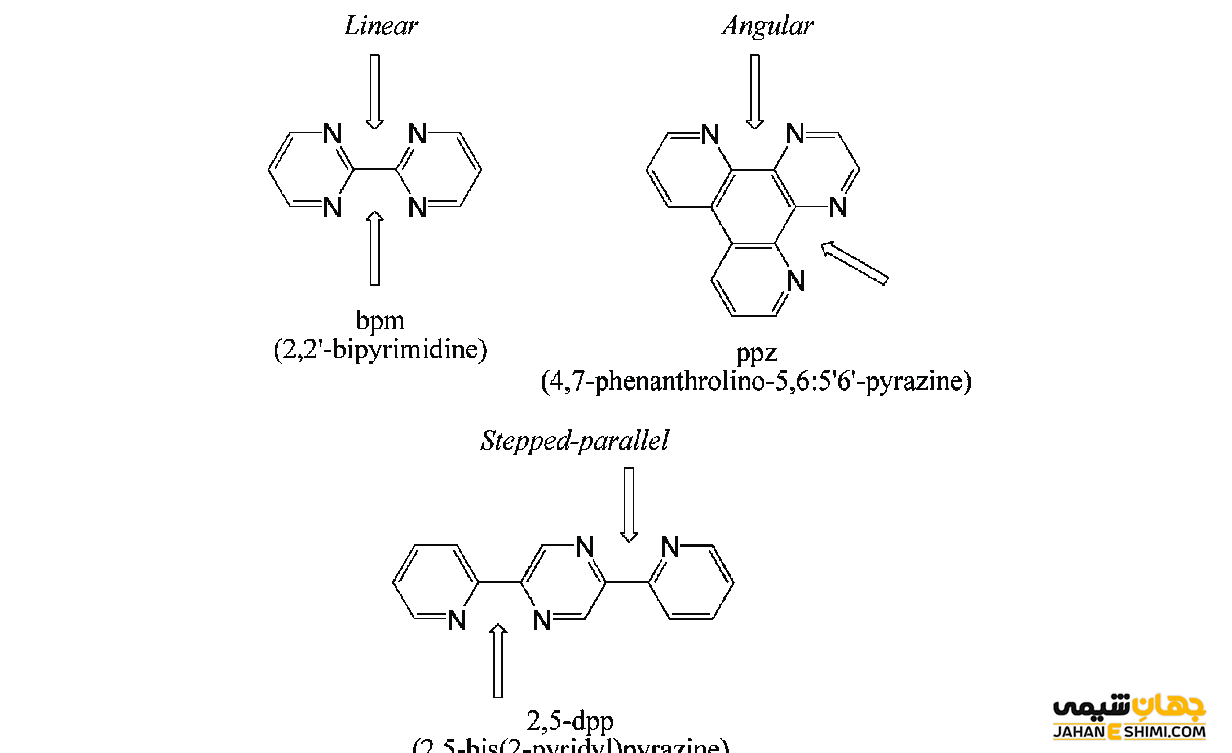
نظریه میدان لیگاند
توصیف خواص کمپلکس های کوئوردیناسی به کمک نظریه میدان لیگاند توصیف می شود که به نام هندسه کمپلکس نیز نامیده می شود. با ترکیب دو نظریه میدان بلور و نظریه اوربیتال مولکولی، نظریه میدان لیگاند بیان شده است. این نظریه بیان می کند که وقتی پوششی از لیگاندهای مجاور، اوربیتال های مختلف d را فرا می گیرد، اوربیتال های مذکور متاثر می شوند. در نتیجه با توجه به میزان نیروی برهمکنشی که اوربیتال ها با لیگاندها دارند، افزایش و یا کاهش انرژی آن ها صورت می گیرد.
کمپلکس کوئوردیناسی
ترکیباتی مانند مس (ll) سولفات نشان دهنده یک ترکیب کمپلکس کوئوردیناسی است. این ترکیب از یک اتم و یا یون به عنوان ذره مرکزی تشکیل می شود. در آن ها لیگاندها به صورت مولکول ها و یون هایی در اتصال با این اتم مرکزی در پیوند هستند. ذره مرکزی نیز به طور معمول یک فلز خواهد بود. ترکیباتی که به طور معمول از فلزات واسطه تشکیل می شوند، به صورت کمپلکس های کوئوردیناسی هستند.
در این ترکیبات در لیگاند، اتمی است که نقش دهنده جفت الکترون خود را به اتم فلز مرکزی بر عهده دارد، این اتم به نام اتم دهنده نامیده می شود.
اما به یون مرکزی همراه با تمام لیگاندهایی که در اتصال به آن هستند، کره کمپلکس می گویند.
در یک ترکیب کوئوردیناسی به به پیوندهای میان لیگاند و اتم مرکزی نیز کوئوردیناسیون گفته می شود.
اما تعدادی از اتم و یا یون هایی که فلز مرکزی توانایی برقرار کردن پیوند با آن ها را دارند، به نام عدد کوئوردیناسیون و یا هم آرایی نامیده می شوند. تعداد اعداد کوئوردیناسی ۲، ۴ و یا ۶ است.
تعریف لیگاند در بیوشیمی و فارماکولوژی
ماده ای در بیوشیمی و فارماکولوژی که با یک مولکول زیستی و یا یک گیرنده در پیوند است و این ترکیب برای انجام یک واکنش و یا هدف بیوشیمیایی خاصی تشکیل می شود، به نام لیگاند نامیده می شود. از لیگاند در عمل بیوشیمی به عنوان یک عمل کننده و ماشه یاد می کنند. این ماده با پروتئین خاصی جفت شده و ترکیبی شیمیایی را برای رسیدن به هدف بیوشیمیایی خاص دنبال می کند. ترکیبات تشکیل شده قابل برگشت هستند. این پیوندها را می توان به کلیدی که برای باز کردن یک قفل به کار می رود، تشبیه کرد. نیروهایی که پیوند لیگاند – پروتئین را تشکیل می دهد، پیوند یونی، پیوند واندروالسی و یا پیوند هیدروژنی است.
تفاوت میان رسپتور و لیگاند چیست؟
لیگاند ماده ای است که به رسپتور متصل می شود و در این اتصال، شکل فضایی رسپتور عوض می شود. اما رسپتور که یک پروتئین پلاسمایی و یا غشایی است، با تغییر شکل خود، می تواند واکنش شیمیایی خاصی را انجام دهد. ولی لیگاندها هر نوع مولکولی مانند دارو و یا هورمون هستند. به عنوان مثال آنزیمی که وظیفه فسفریله کردن گلوکز را بر عهده دارد، گلوکوکیناز نامیده می شود و یک رسپتور است. ولی لیگاند آن گلوکز است. پس در یک فرایند بیوشیمیایی و سلولی می توان گفت که رسپتور به عنوان انجام دهنده کار و لیگاند علت انجام کار خواهد بود.



















