جداسازی مخلوط ها با چه روش هایی انجام می شود؟

جداسازی مخلوط می تواند با روش های مختلفی انجام شود. هر مخلوطی از ترکیب دو یا چند جزء تشکیل شده است که اجزای تشکیل دهنده آن می تواند با طرق متفاوتی از هم جداسازی شود. سرریز کردن، صاف کردن، تبلور و تقطیر روش های مختلف جداسازی مخلوط ها است.

جداسازی مخلوط ها را می توان در کتب علوم چهارم و علوم هشتم مشاهده کرد. دانش آموزان برای اولین بار با این فرایندها کتب علوم چهارم و هشتم آشنا می شوند. این مقاله نشریه جهان شیمی فیزیک نیز به ما اطلاعاتی مختصر درباره روش های جداسازی مخلوط ها ارائه می دهد.
مخلوط چیست؟
به ترکیبی که از دو یا چند ماده تشکیل شده که به طور فیزیکی با هم ترکیب شده اند، مخلوط می گویند. این اجزا به طور شیمیایی به هم متصل نبوده و ساختار آن ها در مخلوط ها تغییری نمی کند. به عبارتی اجزای تشکیل دهنده یک مخلوط، خواص اولیه خود را حفظ کرده و به راحتی با روش های مختلف می توانند از هم جدا شوند.
به عنوان مثال مخلوط آب و نمک نمونه ای از یک مخلوط است که آب و نمک به عنوان اجزای تشکیل دهنده آن، خواص شیمیایی اولیه خود را دارند. اما خواص فیزیکی مانند نقطه ذوب مخلوط با نقطه ذوب هر یک اجزا متفاوت خواهد بود. از ویژگی های مخلوط ها نیز می توان به حفظ خواص اصلی اولیه اجزا، جداسازی آسان آن ها و همچنین متغیر بودن نسبت اجزای تشکیل دهنده اشاره داشت.
انواع مخلوط ها
مخلوط ها را می توان به دو دسته ی همگن (یکنواخت) و غیرهمگن (غیریکنواخت) تقسیم بندی کرد.
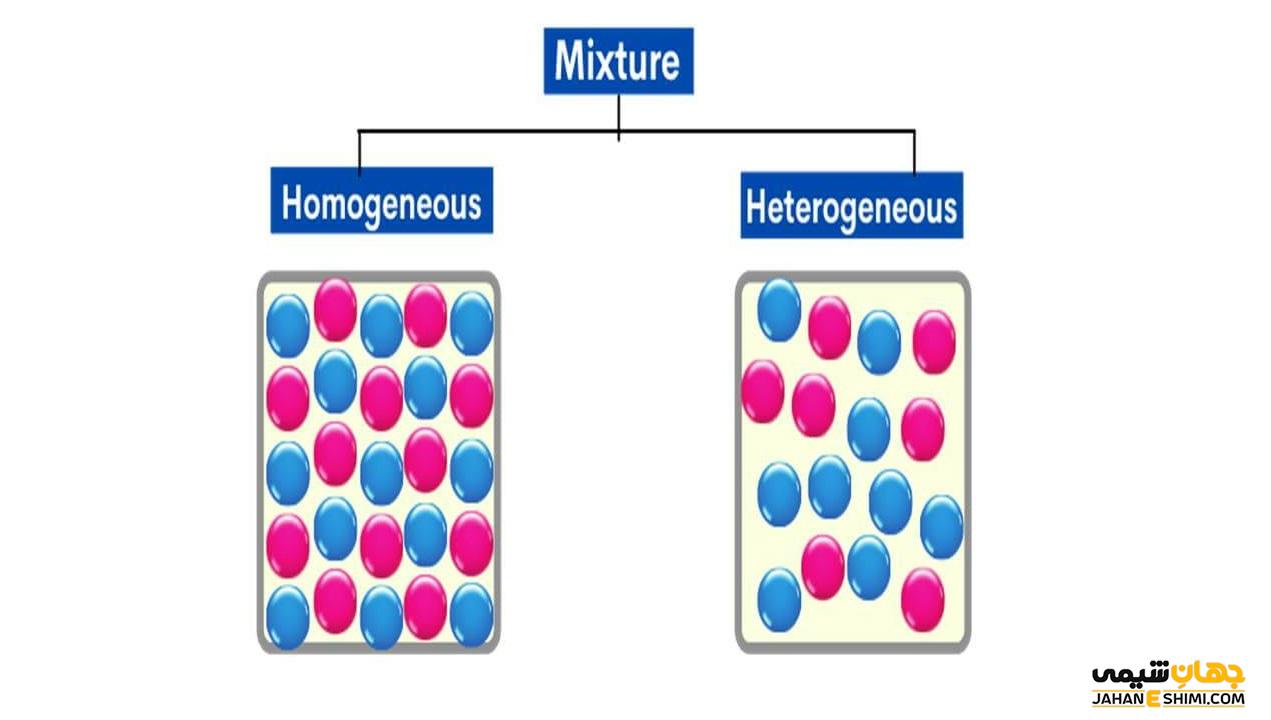
مخلوط غیرهمگن (غیریکنواخت)
به مخلوط هایی که اجزای تشکیل دهنده آن به طور یکنواخت در همه جای آن پخش نشده است، مخلوط ناهمگن گفته می شود. در این مخلوط ها می توان تمام اجزا و یا برخی از آن ها را به راحتی از هم تشخیص داد. به عبارتی در این نوع مخلوط ها، اجزا بدون این که در هم حل شوند، در هم معلق هستند. به عنوان مثال از مخلوط های غیرهمگن مایع در مایع می توان به آب و روغن اشاره کرد. مخلوط ناهمگن جامد در مایع نیز مانند مخلوط نشاسته در آب است. دود در هوا نمونه ای از مخلوط غیریکنواخت جامد در گاز است.
مخلوط همگن (یکنواخت) یا محلول
به مخلوط دیگری که اجزای تشکیل دهنده آن به طور یکنواخت در همه جا پخش شده و این اجزا به آسانی از هم قابل تشخیص نیستند، مخلوط همگن یا یکنواخت گفته می شوند. به مخلوط های همگن، محلول گفته می شود که اجزای تشکیل دهنده آن، حلال و حل شونده است. حلال به جزئی با مقدار بیشتر گفته می شود که جزء حل شونده را در خود حل می کند. ماده حل شونده نیز دارای مقداری کمتر از مقدار حلال بوده و در بین ذرات حلال پخش می شود.
انواع مخلوط های همگن یا محلول ها، جامد در جامد مانند آلیاژ آهن و کربن، جامد در مایع مانند شکر در آب، مایع در مایع مانند الکل در آب، گاز در مایع مانند نوشابه های گازدار و گاز در گاز مانند هوا که مخلوطی از نیتروژن، اکسیژن و گازهای دیگر است، هستند.
روش های جداسازی مخلوط ها
برای این که اجزای تشکیل دهنده انواع مختلف مخلوط ها از هم جداسازی شود می توان از چهار روش صاف کردن، سرریز کردن، تقطیر و تبلور استفاده کرد. در این جا به معرفی این روش ها می پردازیم.
صاف کردن
وقتی اجزای تشکیل دهنده یک مخلوط دارای اندازه های مختلفی باشد، به طوری که یکی از آن ها ریز و دیگری درشت باشد، از صافی و یا غربال های مخصوص برای جدا کردن آن ها استفاده می شود. به عنوان مثال در ساختمان سازی و بنایی از صافی های بزرگ مستطیل شکلی استفاده می شود که سرند نامیده می شود.
اما در آزمایشگاه ها از کاغذهای صافی برای این منظور به کار گرفته می شود. این کاغذها دارای سوراخ های میکروسکوپی بوده و روی قیف های شیشه ای و یا بوخنر در آزمایشگاه قرار گرفته و برای جداسازی مخلوط ها استفاده می شود. صافی هایی که در آشپزخانه ها وجود دارد نیز می تواند برای جدا کردن تفاله ی چای و همچنین آبکش کردن برنج به کار برده شوند.
سرریز کردن
از روش های دیگر جداسازی مخلوط ها می توان به سرریز کردن اشاره داشت. این روش برای مخلوط هایی به کار می رود که دارای یک جزء سبک و یک جزء سنگین هستند. به عنوان مثال در مخلوط آب و روغن که روغن به دلیل سبک بودن پایین تر از آب قرار می گیرد، با سرریز کردن آب، می توان دو ماده را از هم جدا کرد. در آزمایشگاه ها، قیف هایی به نام دکانتور و یا قیف جداکننده وجود دارد که برای جداسازی دو فاز آبی و آلی از هم به کار برده می شوند. شستن حبوبات و برنج نیز در آشپزخانه ها با روش سرریز کردن از هم جداسازی می شود.
تقطیر
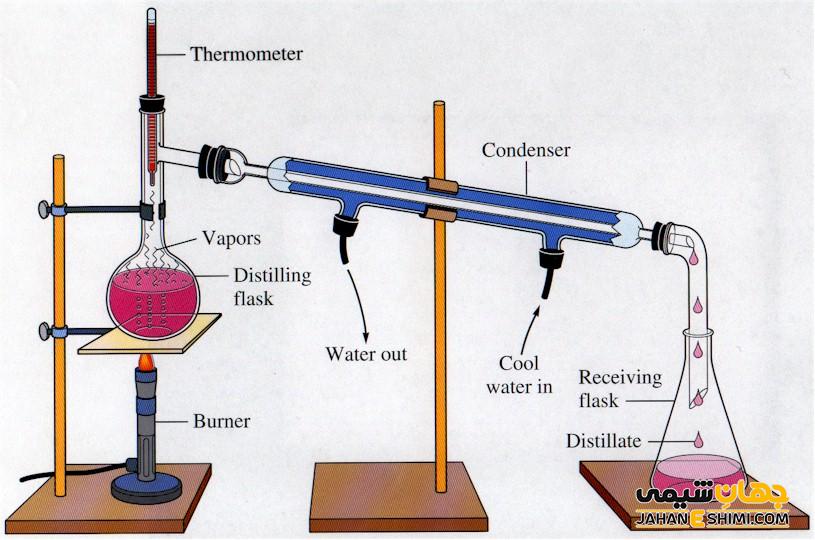
با کمک فرایند تقطیر می توان اجزای یک محلول را بر اساس تفاوت در نقطه جوش این اجزا، از هم جداسازی کرد. این فرایند شامل گرما دادن مخلوط در دمای تعیین شده، جمع کردن بخارات آن و سپس سرد کردن این بخارت و تبدیل آن ها به مایع است. نمونه ای از محلول هایی که با این روش جدا می شوند، محلول مایع در مایع مانند الکل در آب است. این روش به عنوان یکی از روش های خالص کردن مواد نیز به شمار می رود. حتی نقطه جوش برخی از مایعات را نیز با این روش تعیین می کنند.
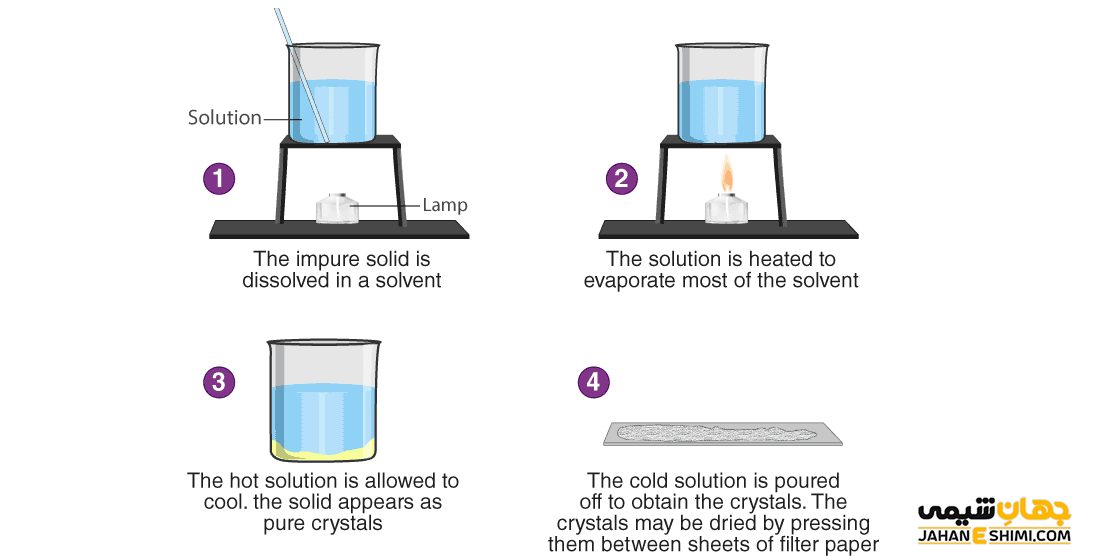
تبلور
وقتی یک ماده شیمیایی در یک محلول به جامد و یا کریستال تبدیل می شود، تبلور رخ داده است. به طور کلی به جداسازی ماده حل شونده از محلول بر اثر سرد شدن، تبلور گفته می شود. در این فرایند ذرات جهت یافته و به آرایش مولکولی منظمی رسیده و این نظم تثبیت می شود. در این فرایند ابتدا یک ذره اولیه جامد به عنوان هسته تشکیل شده و مولکول های بعدی به صورت خوشه ای به طور مشخص جمع می شوند. برای تهیه ی نمک از آب دریا از روش تبلور استفاده می کنند.
در این جا فرایندهای جداسازی مخلوط ها به روش تقطیر و تبلور را بیشتر مورد بررسی قرار می دهیم.
انواع تقطیر
تقطیر ساده
با تقطیر ساده می توان ترکیب را با استفاده از فرایند تبخیر و بخار کردن جداسازی کرد. در این فرایند بخارات ایجاد شده در مرحله های مختلف و ورود به چگالنده، با پدیده میعان به مایع تبدیل می شود. از تقطیر ساده برای جداسازی ترکیب مایعاتی استفاده می شود که اختلاف نقطه جوش اجزای تشکیل دهنده آن، فاصله زیادی درحدود ۷۰ درجه سانتی گراد باشد. همچنین این روش تقطیر برای مخلوط هایی که روغن و یا قسمت های غیرفرار جامد داشته باشد نیز به کار برده می شود. اگر میزان ناخالصی در ترکیبات خالصی که کمتر از ۱۰ درصد باشد با استفاده از روش تقطیر ساده خالص سازی می شود.
با استفاده از تقطیر ساده می توان آب خالص را از آب های سخت تهیه کرد. در تهیه عطر، نوشیدنی های الکلی و صابون به طور سنتی از این روش استفاده می شود.
تقطیر جزء به جزء
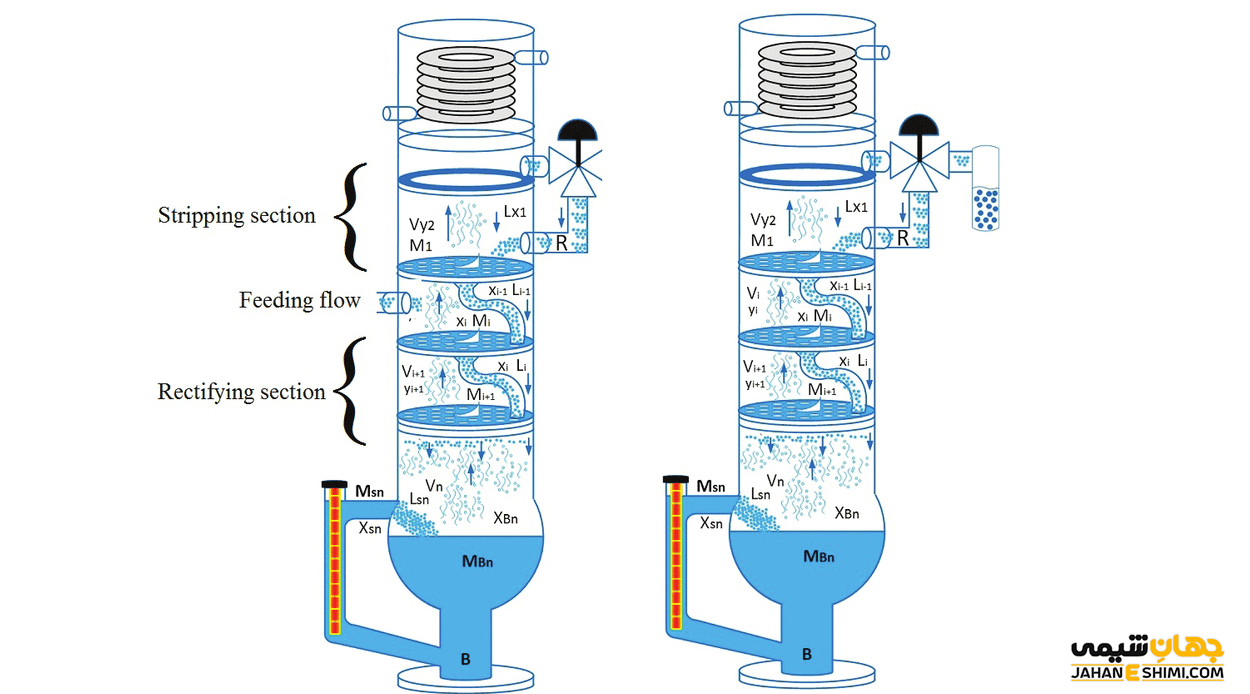
مخلوط هایی که اجزای تشکیل دهنده آن ها، نقطه جوش نزدیک به هم داشته و با روش تقطیر ساده از هم جدا نمی شوند، از تقطیر جزء به جزء به کار گرفته می شود. در این روش اجزای تشکیل دهنده به ترتیب نقطه جوش خود، بخار می شوند و در ستون های برج تقطیر بالا رفته و جداسازی انجام می شود. مسیر انواع ستون های تقطیر، عمودی بوده و عبور ترکیبات در این فرایند از روی سینی هایی صورت می گیرد. در قسمت پایینی ستون تقطیر، اجزا با نقطه جوش بیشتر و در نقاط بالایی ستون تقطیر، اجزا با نقطه جوش کمتر جمع می شوند. این روش تقطیر از پرهزینه ترین روش های تقطیر بوده و در صنعت نفت برای تصفیه الکل و بنزین به کار برده می شود.
جداسازی با روش خلأ
انجام فرایند جداسازی در فشاری پایین تر از فشار استاندارد انجام شده و جوشیدن محلولی که در این روش استفاده می شود در دمایی پایین تر از دمای جوش آن صورت می گیرد. به همین دلیل ترکیباتی که نقطه جوش بالا داشته و ممکن است در دمای جوش خود تجزیه شوند، با کمک این روش جداسازی می شوند. یکی از خواص این روش، انجام بدون گرم کردن است. در صورتی که برای روش های دیگر، با عدم گرما دادن امکان انجام وجود ندارد. یکی از مزیت های این روش، ترکیب آن با روش های دیگر برای عملکرد بهتر است. روش جداسازی با بخار همراه با جداسازی با خلأ برای ترکیبات معطر استفاده می شود.
تقطیر به روش بخار
موادی که حساسیت بالای دمایی و گرمایی دارند مانند ترکیبات آلی با روش تقطیر با بخار جداسازی می شوند. ترکیبات حساس به دما قبل از تجزیه می توانند با این روش جداسازی شوند. در محلولی که از این فرایند به دست می آید، آب و ترکیب خالص است که می تواند با استفاده از تقطیر ساده از هم جدا شود و بخارات جمع شده متراکم شود. در جدا کردن عطرها، روغن ها و چربی ها از تقطیر بخار استفاده می شود.
تقطیر پیوسته
یکی از روش های تقطیر معمول در صنعت، تقطیر پیوسته است که به طور مداوم خوراک به ستون وارد می شود. در این روش استفاده از نیروی انسانی و مراقبت کمتر است زیرا شرایط عملیاتی خاصی برای یک نوع خوراک تعیین می شود. مهمترین مزیت این روش تقطیر مقرون به صرفه بودن آن است.
تقطیر ناپیوسته
در روش تقطیر ناپیوسته، محلول به صورت ناپیوسته و گروهی به ستون تقطیر وارد می شود. بعد با اجرای فرایند جداسازی، اجزای تشکیل دهنده ترکیب از هم جداسازی می شود.
تقطیر به روش مسیر کوتاه
در این روش جداسازی گرمایی در فشار بین ۰,۰۰۱ تا ۱ میلی بار انجام می شود. یکی از خصوصیات این روش این است که ترکیبات جدا شده متراکم می شوند بدون این که به کندانسور منتقل شوند. جای کندانسور در فضای بین فلاسک گرمایی و فلاسک جمع آوری کننده است. ترکیباتی در این روش جداسازی می شوند که وزن مولکولی بالایی دارند. در داروسازی و همچنین تهیه روغن های خوراکی و چربی از این روش تقطیر استفاده می شود.
انواع تبلور
ایجاد تبلور با تبدیل حالت مایع به جامد
این حالت تبلور به دو شکل انجماد مواد مذاب و تبلور مواد محلول انجام می شود.
منجمد شدن مواد مذاب
در انجماد مواد مذاب، متراکم شدن اتم ها و مولکول ها با هر موقعیت و مکانی که دارند، صورت می گیرد. جسم جامدی که در نتیجه ی این انجماد شکل می گیرد، بی نظم است. با سرد شدن آرام و کند، مولکول ها در کنار هم قرار می گیرند و اولین ذره بلوری را تشکیل می دهند. این تشکیل بلور بر اساس نیروی جاذبه مولکول ها و پیروی از شبکه بلوری تشکیل می شود. بعد از تشکیل اولین ذره، مولکول های معلق دیگر به این ذره متصل شده و حجم بلور بزرگتر می شود.
انجماد مواد محلول
در تبلور محلول، فوق اشباع شدن صورت گرفته و بلورها ته نشین می شوند. در این جا نیز، ذره اولیه تشکیل می شود ولی به صورت متحرک است. متحرک بودن یون ها و مولکول های سازنده، علت متحرک بودن این ذره اولیه است. سپس بعد از اتصال منظم یون ها، اتم ها و مولکول های معلق به ذره اولیه، حجم بلورها بزرگتر می شود.
ایجاد تبلور با تبدیل حالت بخار به جامد
در این حالت بلوری شدن، بخار به طور مستقیم به جامد تبدیل شده و اندازه آن ها کوچک است. در این بلورها طرح اولیه ای است که اسکلت بلور خوانده می شود. این حالت بلوری را در طبیعت می توان در گازهای خشک آتشفشانی مشاهده کرد. نمونه ای آشکار دیگر این حالت انجماد، تشکیل بلورهای یخ روی شیشه پنجره اتاق هاست که در زمستان ناشی از منجمد شدن مستقیم بخار آب است.
تبلور مواد جامد
یکی دیگر از انواع تبلور، در محیط جامد صورت می گیرد. با بلورهای کوچک، با فشار و حرارت و به مدت طولانی، بزرگتر شدن بلورها صورت می گیرد. نمونه ای از این نوع متبلور شدن، سنگ های شیشه ای آتشفشانی خیلی کهنه و قدیمی است. این نوع سنگ ها در مدت زمان طولانی و به کندی بلوری شده اند. به عنوان مثال تبدیل سنگ های آهکی دانه ریز متشکل از کربنات کلسیم به مرمر متشکل از بلورهای کلسیت درشت بلوری است. این تبدیل به وسیله عوامل دگرگونی چون فشار و حرارت صورت می گیرد.
دستگاه های جداسازی مخلوط ها
یک مخلوط از دو یا چند نوع ماده تشکیل شده است که می توانند در مقادیر مختلف وجود داشته باشند و با استفاده از روش هایی که از خواص فیزیکی برای جداسازی اجزای مخلوط استفاده می کنند، مانند تبخیر، تقطیر، فیلتراسیون و کروماتوگرافی، می توان آنها را به صورت فیزیکی جدا کرد.
مخلوط ها را می توان با استفاده از روش های مختلف و دستگاه های جداسازی مانند فیلتراسیون، قیف جداکننده، تصعید، تقطیر ساده و کروماتوگرافی کاغذی جدا کرد. روش های ذکر شده در بالا همه روش های فیزیکی هستند. روش های شیمیایی نیز وجود دارد که با مرتب کردن مجدد ذرات استفاده می شود تا ماده خاصی دیگر وجود نداشته باشد (واکنش شیمیایی). با این حال در اینجا در مورد چهار روش فیزیکی اصلی جداسازی توضیح می دهیم.
تقطیر
اگر دو ماده نقطه جوش متفاوتی دارند و با هم مخلوط می شوند، می توانید آنها را بجوشانید و ماده ای که نقطه جوش کمتری دارد تبخیر می شود. این عمل در دستگاه تقطیر صورت می گیرد.
کروماتوگرافی
اگر تا به حال آزمایش هایی را انجام داده اید که در آن نقاط رنگی را روی دستمال کاغذی بکشید و آن را در آب فرو کنید، این همان کرماتوگرافی است. کروماتوگرافی زمانی است که یک ماده (در این مورد از طریق حوله) منتقل می شود یا با جذب آب به اطراف پخش می شود. اکنون انواع مختلفی از دستگاه های کروماتوگرافی در صنعت و آزمایشگاه برای جداسازی مخلوط ها و سنجش های مختلف استفاده می شود.
تبلور
برای یک محلول فوق اشباع، می توانید تبلور املاح استفاده کنید. در این روش آب نبات سنگی یا نبات را می توانید از محلول شکر به دست بیاورید.
فیلتراسیون / آب دهی.
با استفاده از یک غشای انتخابی مانند کاغذ صافی می توانید مخلوط ها را بر اساس اندازه ذرات جدا کنید. از فیلتراسیون می توان برای جداسازی کربنات کلسیم (گچ) از آب استفاده کرد.



















