نام گذاری ترکیبات شیمیایی چیست؟ – قواعد آیوپاک

به قوانینی که توسط آیوپاک برای مولکول های مختلف وضع شده است تا درک راحت تر و بهتری با نوشتارهای آن داشته باشیم، قوانین نام گذاری ترکیبات شیمیایی می گویند. دو دسته از مواد در شیمی وجود دارد که به نام های ترکیبات آلی و معدنی هستند. نام هایی که در گذشته برای ترکیبات شیمیایی بیان می شد، با توجه به ساختار ظاهری و ویژگی های آن ها و گاه کاربردهای آن ها بود. ولی امروزه با قوانین مشخص و خاصی می توان تمام ترکیبات شیمیایی را نام گذاری کرد. این مقاله نشریه جهان شیمی فیزیک ما را با قوانین نام گذاری ترکیبات شیمیایی آشنا می کند.
نام گذاری ترکیبات شیمیایی
همان طور که اشاره شد در گذشته برای نام گذاری ترکیبات شیمیایی از خواص و کاربرد آن ها استفاده می شد. به عنوان نمونه گاز خنده، سنگ آهک، شیر منیزی و سود سوزآور از این نوع نام گذاری ها هستند. برخی از این نام ها امروزه نیز به کار برده می شوند. همچنین قبل از این که آیوپاک قوانین را وضع کند، متناسب با سلیقه کاشف، ترکیبات جدید را نام گذاری می کردند. این نام گذاری ها در زمان های اولیه که شیمی به عنوان علمی جوان شناخته می شد، به کار برده می شد. اما بعد از پیشرفت و گسترده شدن شیمی و افزایش تعداد ترکیبات شناخته شده، شیمی دان ها به دنبال قوانینی گشتند تا این نام گذاری ها راحت تر باشد و به خاطر سپردن آن ها اسان باشد.
در نام گذاری های جدید از اعداد رومی و یونی استفاده می شود. به عنوان مثال برای عدد یک، عدد رومی به صورت I و عدد یونانی به صورت مونو نوشته می شود. در نام گذاری ترکیبات شیمیایی به تفکیک آن ها به دو دسته ترکیبات معدنی و آلی می پردازیم.
نام گذاری ترکیبات شیمیایی معدنی
به ترکیبات غیرآلی، ترکیبات معدنی می گویند. در این جا به نام گذاری دسته های مختلف ترکیبات شیمیایی معدنی می پردازیم.
نام گذاری ترکیبات شیمیایی یونی
ترکیبات یونی مختلفی در پوسته زمین وجود داشته و همچنین در ترکیب مواد غذایی نیز این مواد یافت می شوند. از مواد یونی پوسته زمین می توان به سنگ آهک و خاکستر سودا و از ترکیبات یونی موجود در مواد غذایی می توان به کلرید سدیم و کربنات کلسیم اشاره کرد. در کل ترکیبات یونی از برقراری پیوند بین کاتیون ها و آنیون ها تشکیل شده اند. فرمول ترکیبات یونی را که اکثر آن ها خنثی هستند می توان با توجه به عناصر تشکیل دهنده آن ها نوشت.
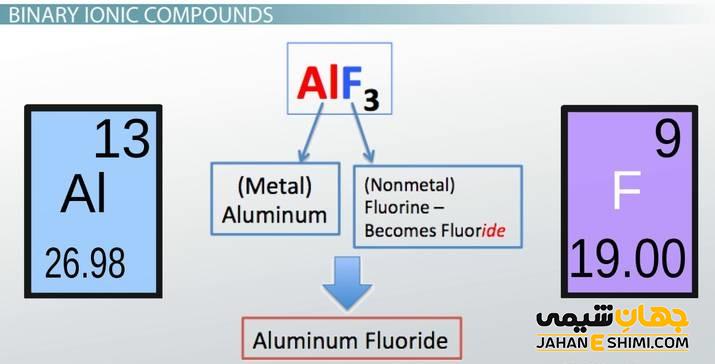
ترکیب یونی چیست؟
یکی از مهمترین ترکیبات یونی که در زندگی روزمره با آن سروکار داریم، نمک خوراکی است که به نام سدیم کلرید مشهور است. این ترکیب از کاتیون سدیم و آنیون کلر که با پیوند قوی یونی به هم متصل هستند، تشکیل شده است. نسبت این یون ها در ترکیب سویم کلرید به صورت یک به یک است.
یکی از مهمترین ویژگی های ترکیبات یونی، برابر بودن مجموع بارهای مثبت و منفی در آن هاست. همچنین در فرمول این ترکیبات باید کوچک ترین نسبت ممکن بین یون ها برقرار باشد. با این که این ترکیب به نام نمک خوراکی است، ولی در صورت فراموشی نام آن، از نام فرمول شیمیایی که با توجه به قانون آیوپاک نوشته می شود استفاده می شود.
معمولا برای تشکیل یک ترکیب یونی، فلزات با نافلزات به واسطه از دست دادن و یا گرفتن الکترون ترکیب می شوند. به عبارتی، فلزات الکترون از دست داده و تشکیل کاتیون می دهند. نافلزات نیز الکترون گرفته و تشکیل آنیون می دهند. بین آنیون ها و کاتیون ها پیوند قوی یونی برقرار می شود.
نام گذاری کاتیون ها
در نام گذاری کاتیون ها از نام عنصر سازنده آن استفاده می شود. اما در این مورد، استثنایی به نام یون آمونیوم وجود دارد که از این قوانین تبعیت نمی کند. به عنوان مثال، Na+ را به نام یون سدیم برگرفته از عنصر سدیم نام گذاری می کنند.
نام گذاری ترکیبات یونی دوتایی
اما وقتی یک ترکیب شیمیایی از دو عنصر تشکیل شده باشد، برای نام گذاری آن ابتدا نام عنصر کاتیون و سپس نام عنصر آنیون ذکر می شود. اما پسوند «ید» به آخر نام آنیون اضافه می شود. نمک خوراکی با فرمول NaCl مثالی از این مورود است که به نام سدیم کلرید خوانده می شود. نمونه هایی از آنیون ها و نام گذاری آن ها در ترکیبات یونی، نیترید، فلوئورید، برمید، کلرید، اکسید، کاربید و سلنید هستند.
نام گذاری ترکیبات شیمیایی یونی که بیشتر از یک نوع کاتیون دارند
همان طور که می دانیم یکی از خواص فلزات واسطه، داشتن چند عدد اکسایش در آن هاست. این خصوصیت سبب شده که این فلزات بتوانند بیشتر از یک کاتیون تشکیل دهند. آهن، مس، کروم، کبالت و منگنز مثال هایی از این فلزات هستند. در این شرایط برای نام گذاری آن ها از اعداد رومی استفاده می شود. روش نام گذاری به این شکل را به نام روش استاک می خوانند. در این نام گذاری، کاتیون با بار مثبت کمتر با پسوند «اوس» و کاتیون با بار مثبت بیشتر با پسوند «یک» نوشته می شود. به عنوان مثال به یون Fe۲+ یون فروس و به یون Fe۳+ یون فریک می گویند.
اما در این نوع نامگذاری نمی توان بار یون ها را از روی نام آن ها متوجه شد. همچنین این نام گذاری، فقط برای عناصر دو کاتیونی استفاده می شود. در صورتی که برخی از فلزات بیشتر از دو نوع کاتیون دارند. به همین دلیل است که اعداد رومی برای نام گذاری آن ها استفاده می شود. در این روش، عدد رومی به ازای هر بار مثبتی که روی کاتیون است، به کار برده می شود.
پس نام گذاری با این روش به این ترتیب می شود که ابتدا نام کاتیون نوشته شده و داخل پرانتز عدد رومی مربوط به بار کاتیون نوشته می شود. سپس نام آنیون به اضافه پسوند «ید» وارد می شود. به عنوان مثال نام MnO به صورت منگنز(ll) اکسید نوشته می شود.
نام گذاری ترکیبات یونی سه تایی و چندتایی
در این ترکیبات نیز از پسوند «ید» برای نام گذاری گروه های آنیونی استفاده می شود. مثال هایی از این آنیون ها، هیدروکسید و سیانید هستند که از دو عنصر تشکیل شده اند. وقتی این آنیون ها در کنار کاتیون ها قرار می گیرند، ترکیب سه تایی تشکیل می دهند. لیتیم هیدروکسید (LiOH) مثالی از این ترکیبات است.
اما زمانی که یون ها از چند عنصر تشکیل شده باشند، ترکیبات چند اتمی تشکیل می شود. یون سولفات (SO۴-۲) مثالی از این یون هاست. سدیم نیتریت (NaNO۲) و آهن (ll) سولفات (FeSO۴) نمونه هایی از این ترکیبات هستند. آمونیوم نیترات (NH۴NO۳) یک ترکیب شیمیایی یونی چند اتمی است.
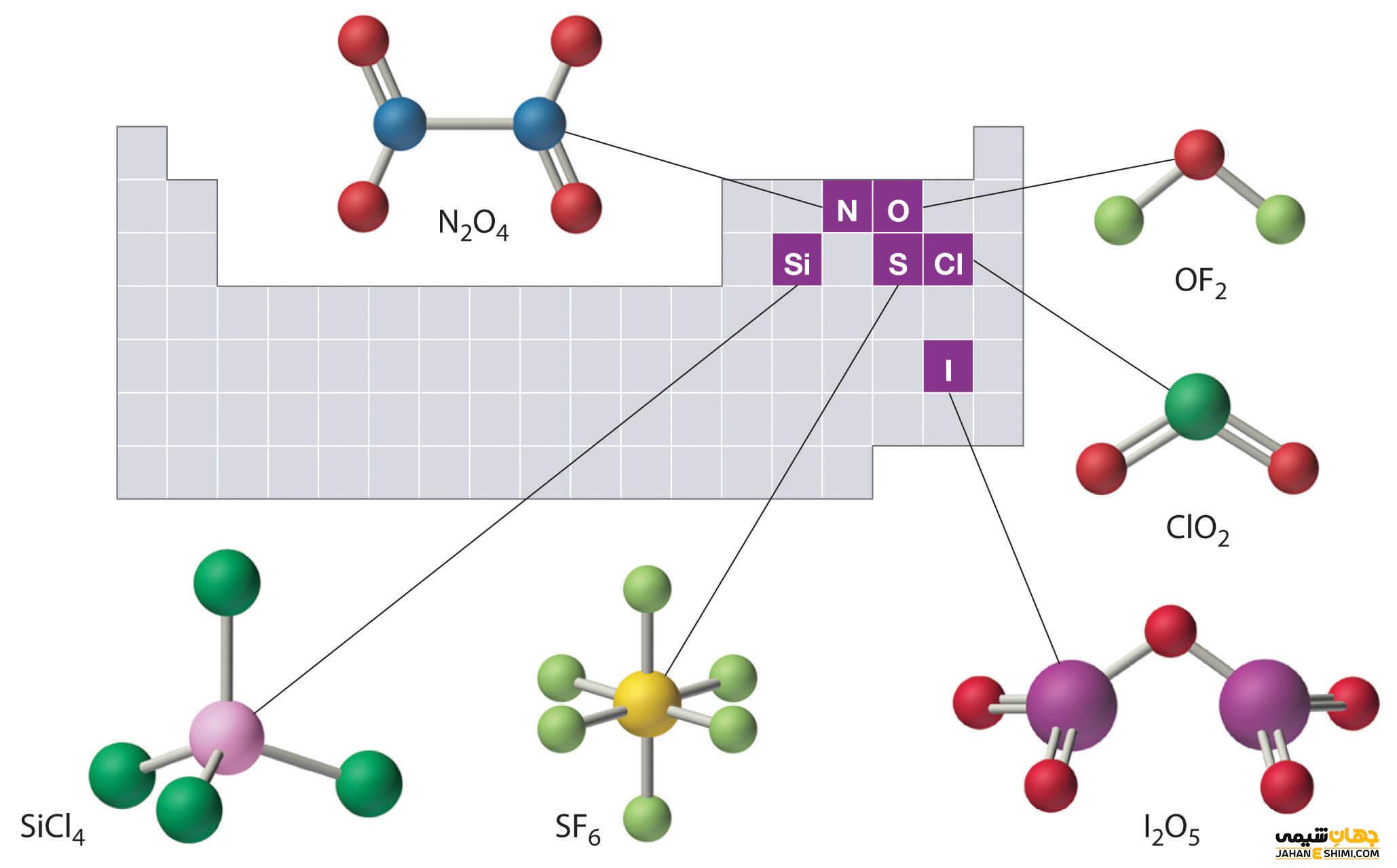
نام گذاری ترکیبات مولکولی
ترکیبات مولکولی از نافلزات تشکیل شده اند که به صورت واحدهای مجزا در کنار هم با پیوندهای مختلفی قرار می گیرند. اگر این ترکیبات به صورت دو مولکولی باشند، مانند یون ها دوتایی، ابتدا نام عنصر اول و سپس نام عنصر دوم با پسوند «ید» آورده می شود. در زمان هایی که دو عنصر یکسان تشکیل ترکیبات متفاوت را دهند، از اعداد یونانی برای نام گذاری آن ها استفاده می شود. به عنوان مثال از ترکیب دو اتم اکسیژن و کربن، ترکیبات مولکولی مختلفی چون کربن مونوکسید (CO)، کربن دی اکسید (CO۲) و از ترکیب دو عنصر گوگرد و اکسیژن نیز ترکیبات مختلفی چون گوگرد دی اکسید (SO۲) و گوگرد تری اکسید (SO۳) حاصل می شود.
فرمول مولکولی
با در دست داشتن نام یک ترکیب مولکولی می توان فرمول مولکلی آن را به راحتی نوشت. به عنوان نمونه وقتی یک ترکیب با نام آرسنیک تری فلوئورید را داریم، در نگاه اول متوجه حضور دو عنصر آرسنیک و فلوئور در آن می شویم. همچنین تعداد اتم آرسنیک، یک و تعداد اتم فلوئور، سه است. با دقت در این نام متوجه می شویم که طبق ترتیب قانون نام گذاری، نام آرسنیک در ابتدا و نام سه اتم فلوئور به صورت عنصر دوم است. در نتیجه فرمول مولکولی آن به صورت AsF۳ است.
نام گذاری ترکیبات کووالانسی
به ترکیباتی که با پیوندهای کووالانسی، عناصر تشکیل دهنده آن در کنار هم قرار گیرند، ترکیبات کووالانسی می گویند. این ترکیبات دقیقا مانند ترکیبات مولکولی نام گذاری می شوند. به عنوان مثال ترکیب SO۲، به نام گوگرد دی اکسید نام گذاری می شود.
نام گذاری ترکیبات کوئوردینانسی
ترکیباتی به نام ترکیبات کوئوردینانسی وجود دارند که در آن ها یک یون فلزی به عنوان اتم مرکزی بوده که در اتصال با چند لیگاند هستند. به طور معمول، یون های مرکزی آن ها فلزات واسطه هستند زیرا این عناصر دوست دارند که ترکیبات کوئوردینانسی را تشکیل دهند. لیگاندها با دادن جفت الکترون، با فلز و اتم مرکزی پیوند برقرار می کنند. به عبارتی برای تشکیل یک ترکیب کوئوردینانسی، یون کمپلکس با یک یا چند یون با بار مخالف ترکیب می شود. نتیجه تشکیل یک ترکیب خنثی است.
در نام گذاری این ترکیبات ابتدا نام کاتیون و سپس نام آنیون نوشته می شود.
نام گذاری لیگاند
لیگاندها نیز به صورت های ویژه ای نام گذاری می شوند. به عنوان مثال برخی از آن ها نام خاصی دارند. اکوا (H۲O) و آمین (NH۳) نمونه ای از این لیگاندهاست. اما لیگاندهای آنیونی با پسوندهای خاصی نام گذاری می شوند. در این روش به جای پسوند «ید»، «و»، به جای پسوند «ات»، «یت» و به جای پسوند «یت»، «یتو» نوشته می شود. به عنوان مثال کلرید به صورت کلرو، سولفات به صورت سولفاتو و سولفیت به صورت سولفیتو نوشته می شود.
در صورت وجود چند لیگاند در نام گذاری ترکیبات کوئوردینانسی، به ترتیب حروف الفبای انگلیسی نام آن ها نوشته می شود. همچنین در صورت یکسان بودن لیگاندها از اعداد یونانی برای نوشن استفاده می شود. نکته سومی که باید دقت کرد، در صورت وجود پیشوند یونانی در نام لیگاند، این نام داخل پرانتز نوشته شده و از بیس (۲)، تریس (۳) و تتراکیس (۴) استفاده می شود.
نام گذاری فلزات
در یون کمپلکس، برای نوشتن نام کاتیون، ابتدا نام فلز و سپس عدد اکسیداسیون به صورت رومی نوشته می شود. اما اگر یون کمپلکس، آنیون باشد، برای نوشتن آن ابتدا نام فلز، بعد پسوند «ات» و سپس عدد اکسیداسیون به صورت رومی داخل پرانتز نوشته می شود.
در نهایت
بعد از این که نام لیگاند و نام فلز در یک یون کمپلکسی نوشته شد، ترتیب نوشتن آن به صورت ابتدا نام لیگاند و سپس نام فلز خواهد بود.
توجه
در نام گذاری ترکیبات شیمیایی نوشتن اسیدها، بازها و هیدرات ها نیز دارای قوانین خاصی هستند.
نام گذاری ترکیبات آلی
به طور مختصر در این مقاله درباره قوانین نام گذاری دسته ای از ترکیبات آلی به نام آلکان ها می پردازیم. به طور کلی ترکیباتی که در ساختار خود اتم کربن داشته و با عناصری چون هیدروژن، اکسیژن، نیتروژن و گوگرد، پیوند دارند، به نام ترکیبات آلی هستند. هیدروکربن ها از ساده ترین ترکیبات آلی هستند که خود به دسته های دیگری تقسیم می شوند.
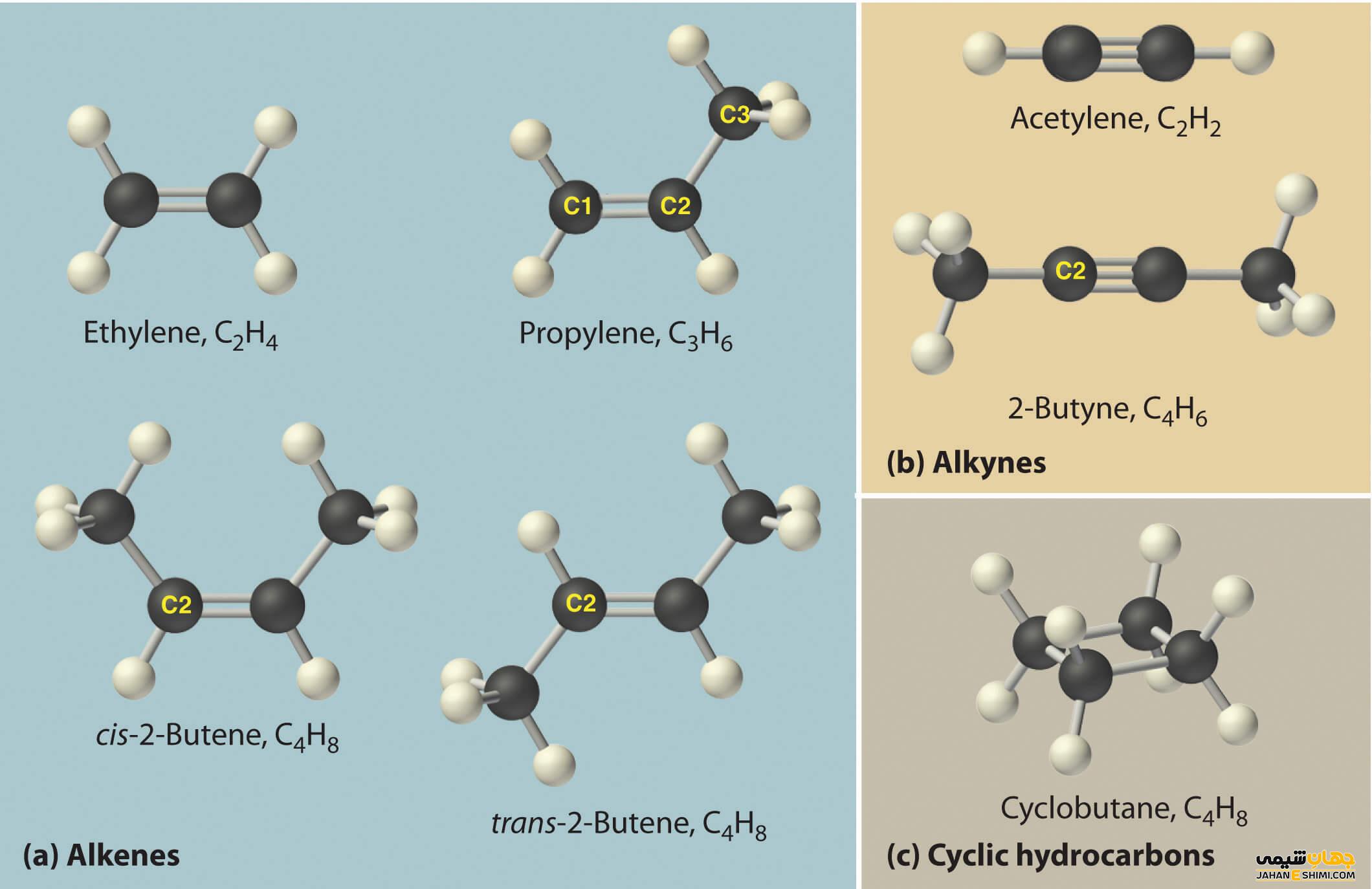
آلکان ها ساده ترین هیدروکربن بوده و برای نام گذاری آن ها قوانین خاصی توسط آیوپاک وضع شده است. در این ترکیبات، ابتدا بلندترین زنجیر کربنی را به عنوان زنجیر اصلی در نظر می گیرند. نام آلکان را با استفاده از پیشوند یونانی آن ها به اضافه پسوند «ان» می نویسند. تعداد کربن زنجیر اصلی به اضافه پسوند «ان» نام آلکلن خواهد بود. آلکین ها و آلکین ها نیز به همین ترتیب هستند با این تفاوت که به جای پسوند«ان» از پسوند «ِاِن» و «ین» استفاده می شود.
اما گاهی تعدادی از اتم های کربن به صورت زنجیر جانبی در این ترکیبات قرار می گیرند که ایزوپروپیل الکل نمونه ای از آن است.
قواعد نام گذاری آلکان ها
ابتدا بلندترین زنجیر کربنی انتخاب شده و شماره گذاری از سمتی آغاز می شود که با گروه های جانبی نزدیکتر باشد. در صورت وجود استخلاف در هر دو سمت، شماره گذاری از استخلاف نزدیکتر انجام می شود. در این شرایط که چند استخلاف وجود دارد، استخلاف ها همراه با اعداد و به ترتیب حروف انگلیسی با خط فاصله بین کلمات و اعداد نوشته می شوند. استخلاف هایی که یکی باشند، تعداد آن ها را با اعداد یونانی نمایش می دهند. مکان و موقعیتی که هر استخلاف روی کربن دارد با استفاده از عدد مشخصی روی آن نوشته می شود. بدون این که پیشوندها در نظر گرفته شود، حروف الفبا مرتب می شوند.
پس برای نام گذاری ابتدا عدد استخلاف، سپس نام استخلاف و در نهایت نام زنجیر اصلی نوشته می شود.



















