
عنصر مایتنریم (Meitnerium) با نماد شیمیایی Mt، یکی از عناصر شیمیایی جدول مندلیف است که عدد اتمی آن ۱۰۹ می باشد. این عنصر در حقیقت صد و نهمین عنصر جدول تناوبی عناصر بوده که در گروه IXB و تناوب هفتم جدول تناوبی عناصر قرار دارد. در واقع عنصر مایتنریوم یک فلز واسطه (Transition Metals) فوق سنگین، مصنوعی و از عناصر با خاصيت راديواكتيو بالای جدول تناوبی است. این فلز با عناصر کبالت (Co)، رودیم (Rh) و ایریدیوم (Ir)، در گروه نه واسطه جدول تناوبی قرار گرفته است. توجه داشته باشید که عنصر مایتنریوم سنگین ترین عضو گروه ۹ می باشد. این عنصر همچنین با نام های میتنریم و میتنریوم نیز شناخته می شود. در ادامه این مقاله در نشریه جهان شیمی فیزیک به بررسی عنصر مایتنریم پرداخته می شود. لطفا با ما همراه باشید.
تاریخچه کشف عنصر مایتنریم
عنصر مایتنریم برای نخستین بار در سال ۱۹۸۲ میلادی توسط يك گروه آلماني به سرپرستی پیتر آرمبروستر (Peter Armbruster) و گاتفرید مونسنبرگ (Gottfried Münzenberg) در موسسه تحقیقات هسته ای یون های سنگین (GSI) واقع در دارمستات، آلمان غربی کشف شد. این محققان عنصر بیسموت (ایزوتوپ ۲۰۹Bi) را با هسته های شتاب دار شده آهن (ایزوتوپ ۵۸Fe) بمباران کردند. بدین شکل موفق به سنتز ایزوتوپ ۲۶۶ از عنصر شماره ۱۰۹ شدند. سنتز این عنصر ثابت کرد که با استفاده از فناوری های همجوشی هسته ای می توان جهت تولید هسته اتم های جدید و سنگین استفاده نمود. این فرآیند سه سال بعد در موسسه مشترک تحقیقات هسته ای در دوبنا (Dubna) که در آن زمان در اتحاد جماهیر شوروی بود تایید شد.

نامگذاری عنصر مایتنریم
گروه آلمانی نام مایتنریوم را به افتخار فیزیکدان و ریاضیدان سوئدی- اتریشی یعنی لیزه مایتنر (Lise Meitner) برای این عنصر پیشنهاد دادند. لیزه مایتنر، در حوزه های فیزیک هسته ای و رادیواکتیویته فعالیت داشت. این دانشمند با همکاری اوتو هان (Otto Hahn) و اوتو رابرت فریش (Otto Robert Frisch)، توانست برای نخستین بار شکافت هسته ای عنصر اورانیوم را در صورت گرفتن نوترون اضافی کشف و ردیابی کند. این محققان فهمیدند که در جریان فرآیند شکافت هسته ای که در طی آن، هسته اورانیوم به دو هسته کوچکتر تقسیم می شود، انرژی زیادی تولید می گردد. این نتایج سبب تولید راکتور های هسته ای به منظور تولید برق و یا حتی تولید بمب هسته ای شد.

برای مدت زمان زیادی، بحث و جدل نامگذاری عناصر ۱۰۱ تا ۱۰۹ جدول تناوبی عناصر وجود داشت. بنابراین، انجمن آیوپاک در ابتدا نام موقت انیلنیم (unnilennium) و نماد Une را برای این عنصر تا زمانیکه یک تصمیم نهایی برای نامگذاری آن گرفته شود، انتخاب کرد. در سال ۱۹۹۴ میلادی، انجمن آیوپاک نام عنصر شماره ۱۰۹ جدول تناوبی را میتنریم پیشنهاد نمود. از آنجاییکه مایتنریم (میتنریوم) تنها پیشنهاد بود، بنابراین هرگز مورد بحث و اختلاف قرار نگرفت. در نهایت و در سال ۱۹۹۷ میلادی، آیوپاک واژه مایتنریم را به عنوان نام رسمی این عنصر تایید کرد.
پیدایش و منابع عنصر شماره ۱۰۹ جدول تناوبی
عنصر مایتنریم به دلیل ناپایداری بسیار بالا در طبیعت وجود ندارد. از این رو، این عنصر در پوسته زمین پیدا نمی شود. در واقع این عنصر به دست بشر و در آزمایشگاه تهیه شده است. به طور کلی می توان گفت که این عنصر از طریق بمباران اهداف بیسموت با اتم های آهن تهیه شده است. لازم به ذکر است که تاکنون تنها تعداد کمی از اتم های مایتنریم ساخته شده است. به احتمال زیاد در آینده نیز هرگز نمی تواند به مقداری ساخته شود که با چشم قابل مشاهده باشد.
به بیان بهتر، اتم های عنصر مایتنریم از طریق هم جوشی میان اتم های بیسموت و آهن بدست آمده است. این کار با شتاب دادن یون های آهن در دستگاه های شتاب دهنده ها انجام شده است. در نهایت و بعد از چند روز، ذرات شتاب دار آهن به سوی هدف بیسموت انتخابی، جهت سنتز عنصر مایتنریم، بمباران شده اند. هسته های آهن (با عدد اتمی ۲۶) و بیسموت (با عدد اتمی ۸۳) در یک واکنش هم جوشی هسته ای با یکدیگر ادغام می گردند. بدین شکل، هسته های عنصر جدید را تشکیل دادند که عدد اتمی آن (۱۰۹) حاصل جمع عدد اتمی دو عنصر آهن و بیسموت خواهد بود. جالب است بدانید که آزمایش فوق نشان داد که استفاده از روش های شکافت (مثل روش ساخت هسته های جدید و سنگین)، ساده می باشد.
سنتز هسته های سنگین
دقت داشته باشید که سنگین ترین هسته های اتمی در واکنش های هسته ای ایجاد می شوند که در طی آن، دو هسته با اندازه نا برابر را در یک هسته ترکیب می شوند. حال هر چه دو هسته از نظر جرم نا برابر تر باشند، احتمال واکنش میان آن دو بیشتر خواهد بود. ماده شیمیایی ساخته شده از هسته های سنگین تر به هدفی تبدیل می شود که می تواند توسط پرتو های هسته های سبک تر بمباران گردد. دو هسته تنها وقتی می توانند با یکدیگر ادغام شوند که به اندازه کافی به هم نزدیک شده باشند. حال اگر انرژی ترکیبی دو هسته نا برابر زیاد باشد، می تواند بر نیرو های دافعه بین هسته ها (هسته ها دارای بار مثبت اند) غلبه کند. پس در این آزمایش به منظور تولید یک هسته منفرد، هدف بایستی یک هفته بمباران می شد.
وقتیکه دو هسته به هم نزدیک می شوند، معمولا به مدت ۱۰ تا ۲۰ ثانیه در کنار هم باقی می مانند، سپس از هم جدا می شوند. اگر همجوشی میان آنها اتفاق افتد، ادغام موقت (که هسته مرکب نام دارد) یک حالت برانگیخته خواهد بود. برای از دست دادن انرژی برانگیختگی و رسیدن به حالت پایدار تر، یک هسته مرکب می شکافد و یا یک یا چند نوترون را بیرون می اندازد. حال اگر انرژی ترکیبی دو هسته نا برابر زیاد نباشد، نیرو های دافعه بین هسته ها بر آن غلبه کرده و واکنش شکست خواهد خورد.
اتم تازه تشکیل شده (با سرعت پیش بینی شده)، از هدف بر می گردد. سپس با فیلتر سرعتی که تازه توسعه یافته بود، از هسته های سریعتر و کوچکتر از خود جدا می شود. در واقع، زمان حرکت به سمت آشکار ساز، مکان و انرژی اندازه گیری می گردد.
ویژگی های فیزیکی و شیمیایی عنصر مایتنریم
همانطور که بیان شد، عنصر مایتنریم تاکنون تنها به مقدار بسیار کمی و در حد چند اتم تهیه شده است. بنابراین اطلاعات کمی درباره شكل ظاهری و یا خواص فیزیکی و شیمیایی آن وجود دارد. با این وجود، تعدادی پیش بینی و نتایج تجربی اولیه در مورد خواص آن انجام شده است. به عنوان مثال، انتظار می رود که مایتنریم یک فلز نجیب باشد.
فلز مایتنریوم در چهارمین و در واقع آخرین دوره بلوک- d جدول تناوبی عناصر واقع شده است. توجه داشته باشید که در این بلوک، هفتمین عنصر است. از طرفی دیگر ششمین عنصر سری ترانس یا فرا اکتینیدی (Transactinide) نیز محسوب می شود. آزمایشات شیمی تاکید کرده اند که عنصر مایتنریوم مانند همولوگ سبکترش یعنی عنصر ایریدیوم در گروه نهم رفتار می کند. عنصر ایریدیوم در خانه بالای مایتنریم در جدول تناوبی قرار دارد.
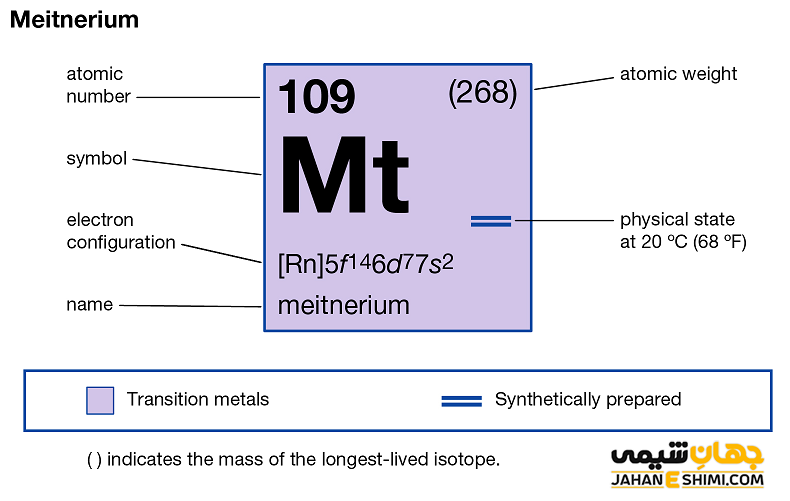
خصوصیات ویژه مایتنریم از ساختار اتمی ([۸۶Rn] 5f۱۴۶d۷۷s۲) آن ناشی می شود. همانطور که از آرایش الکترونی مایتنریم مشخص است، اوربیتال d لایه ماقبل آخر آن در حال پر شدن است. عنصر مایتنریم به واسطه آرایش الکترونی که دارد، در دسته عناصر واسطه قرار می گیرد. فلزات واسطه در بین عناصر قلیایی خاکی و عناصر گروه بور در جدول تناوبی قرار دارند. به عناصر واسطه، عناصر گروه B نیز گفته می شود. با توجه به آرایش الکترونی مشخص است که نه الکترون در دورترین لایه الکترونی آن وجود دارد. پس احتمالا می تواند در ترکیبات شیمیایی به صورت کاتیون نه بار مثبت (+Mt۹) نیز ظاهر شود. از این رو می تواند در نه پیوند کووالانسی شرکت کند.
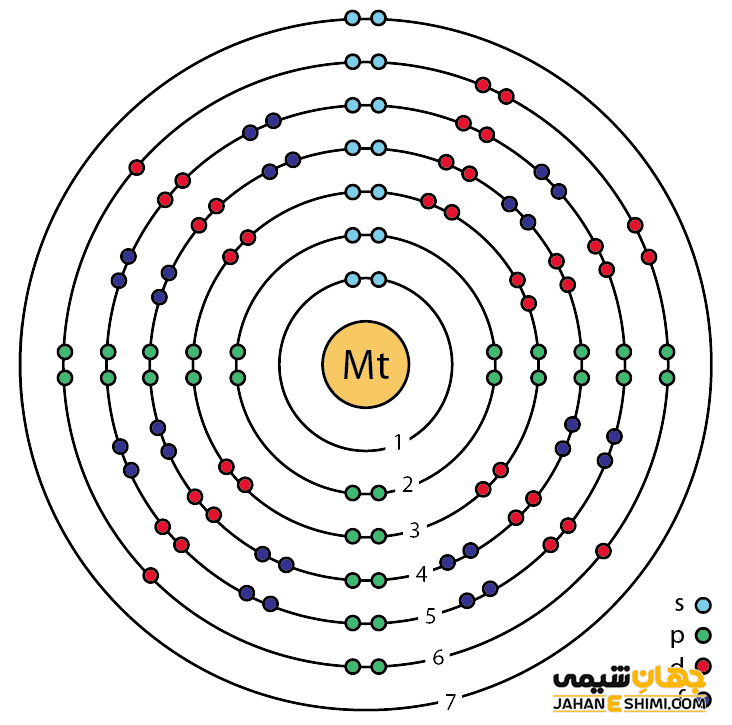
خواص ویژه مایتنریم
لازم به ذکر است که انتظار می رود مایتنریوم نیز همانند سایر هم گروهان خود، بتواند حالت اکسیداسیون پایدار پایین تری مثل ۱+، ۳+ و ۶+ را نیز تشکیل دهد. انتظار می رود که این حالات اکسیداسیون ذکر شده نسبت به مایتنریم ۹+ پایدار تر باشد. علاوه بر آن، حالت اکسیداسیون ۳+ پایدارترین حالت در محلول آبی محسوب می شود. از دیگر ویژگی های عنصر مایتنریوم می توان به موارد زیر اشاره کرد.
- حالت فیزیکی آن در دمای ۲۵ درجه سلسیوس و فشار ۱ اتمسفر احتمالا به صورت جامد است.
- دمای ذوب و دمای جوش این عنصر تعیین نشده است.
- خاصت مغناطیسی عنصر مایتنریم نیز نا مشخص است.
- انتظار می رود که ساختار بلوری آن به شکل مکعبی وجوه پر یا ساختار مکعبی مرکز سطحی (fcc) باشد.
- این عنصر احتمالا آلوتروپ ندارد. در واقع ناشناخته هستند.
- جرم اتمی مایتنریم برابر با ۲۸۲ g/mol است.
- چگالی آن نیز برابر با ۲۷–۲۸ g/cm۳ پیش بینی می شود.
- شعاع اتمی آن نیز ۱۲۸ pm تخمین زده شده است.
- یون های مایتنریم معمولا عدد اکسایش برابر با اعداد ۰، +۱، +۳، +۴، +۶، +۸ و+۹ را دارند. اعداد اکسایش ۰، +۱، +۳ و +۶ متداول تر می باشند.
- انرژی یونیزاسیون آن برابر با ۸۰۰ kJ/mol است.
ایزوتوپ های عنصر مایتنریم
همانطور که در مقالات پیشین نشریه جهان شیمی فیزیک بیان شده است، ایزوتوپ های یک عنصر تنها در تعداد نوترون ها با یکدیگر تفاوت دارند. عنصر مایتنریم ایزوتوپ های فراوانی دارد. نخستین ایزوتوپ شناسایی شده آن، رادیو ایزوتوپ ۲۶۶Mt است که در سال ۱۹۸۲ میلادی کشف شد. از آنجاییکه عنصر مایتنریوم، عنصری مصنوعی است، بنابراین ایزوتوپ پایدار ندارد. این عنصر در حقیقت به صورت سنتزی و در رآکتور های هسته ای تهیه شده است. در نتیجه نمی توان برای آن جرم اتمی استاندارد تعریف کرد. تاکنون ۸ ایزوتوپ پرتوزا از عنصر مایتنریم شناسایی شده است.
لازم به ذکر است که ایزوتوپ های سنگین تر مایتنریم از ایزوتوپ های سبک تر پایدارتر هستند. رادیو ایزوتوپ ۲۷۸Mt پایدار ترین ایزوتوپ مایتنریم با نیمه عمر ۸ ثانیه است. به نظر می رسد که ایزوتوپ رادیواکتیو تایید نشده ۲۸۲Mt، نیمه عمر طولانی تری داشته باشد یعنی در حدود ۶۷ ثانیه. بقیه ایزوتوپ های پرتوزای آن، نیمه عمری کمتر از چند ثانیه دارند. علاوه بر آن، مایتنریوم دارای ۲ حالت متا (m) یا ایزومر هسته ای نیز می باشد (۲۶۸mMt و ۲۷۰mMt). ایزوتوپ های رادیواکتیو این عنصر دارای جرم های اتمی در محدوده ۲۶۶ تا ۲۷۸ amu می باشند.

کاربرد های عنصر مایتنریم
از آنجاییکه عنصر شماره ۱۰۹ جدول تناوبی به میزان بسیار ناچیز (فقط تعداد کمی از اتم های آن) تولید شده است، بنابراین کاربرد خاصی خارج از پژوهش های علمی، هسته ای و یا تحقیقاتی ندارد. به بیان دیگر، به دلیل نیمه عمر پایین مایتنریم، این عنصر کاربرد تجاری ندارد.
ترکیبات عنصر مایتنریوم
پیش بینی می شود که عنصر مایتنریوم بتواند به راحتی با عناصر اکسیژن و هالوژن ها واکنش دهد. در نتیجه اکسید، هالید ها و یا حتی اکسی هالید را تولید نماید. از جمله ترکیبات آن می توان به کاتیون تتروکسید مایتنریم (+[MtO۴]) و نونا فلورئید مایتنریم (MtF۹) اشاره کرد.

خطرات مایتنریم بر روی سلامتی انسان
همانطور که بیان شد، عنصر مایتنریم در طبیعت وجود ندارد. بنابراین در پوسته زمین نیز یافت نشده است. به علاوه، مایتنریم آن قدر ناپایدار است و نیمه عمری کوتاهی دارد، که هر مقداری از آن تشکیل شود، به سرعت به سایر عناصر تبدیل می گردد. بنابراین دلیلی برای در نظر گرفتن اثرات و خطرات سلامتی آن وجود ندارد. به عبارت دیگر، عنصر شماره ۱۰۹ جدول تناوبی نقش زیست شناختی مشخصی ندارد، اما با توجه به پرتوزا بودن، سمی محسوب می شود. بنابراین در هنگام کار با آن، باید حتما مراقب بود.



















