
عنصر نپتونیم (Neptunium) با نماد شیمیایی Np، یکی از عناصر شیمیایی جدول مندلیف است که عدد اتمی آن ۹۳ می باشد. این عنصر در حقیقت نود و سومین عنصر از جدول تناوبی بوده که در گروه IIIB و تناوب هفتم جدول تناوبی قرار دارد. در واقع عنصر نپتونیم یک فلز واسطه (Transition Metals) رادیواکتیو به رنگ نقره ای و از عناصر گروه اکتینید ها است. این فلز با عناصر اسکاندیم (Sc)، ایتریم (Y) و لانتان (La)، در گروه سوم واسطه جدول تناوبی قرار گرفته است. دقت داشته باشید که این عنصر با نام نپتون نیز شناخته می شود. در ادامه این مقاله در نشریه جهان شیمی فیزیک به بررسی عنصر نپتونیوم پرداخته می شود. لطفا با ما همراه باشید.
تاریخچه کشف عنصر نپتونیم
عنصر نپتونیم برای اولین بار در سال ۱۹۳۴ میلادی، توسط شیمیدان ایتالیایی یعنی انریکو فرمی (Enrico Fermi) گزارش شد. وی تلاش می کرد تا از طریق بمباران اتم های اورانیم با نوترون، عناصر شماره ۹۳ و ۹۴ جدول تناوبی را تولید کند. فرمی ادعا داشت که موفق به انجام این کار شده است. وی نام اوسونیوم (ausonium) با نماد شیمیایی Ao، را برای این عنصر جدید انتخاب کرد. البته آیدا نوداک (Ida Noddack) و گروس (Aristid von Grosse) ادعای فرمی را مورد تردید قرار دادند. این دو دانشمند مدعی بودند که فرمی بررسی کاملی انجام نداده است. در واقع هر آنچه که فرمی یافته بود، فقط محصولات شکافت هسته ای اورانیم است. در حقیقت وی بدون آنکه بداند، توانسته بود شکافت هسته ای را کشف کند.

در سال ۱۹۳۸ میلادی، فیزیکدان رومانیایی هوریا هولوبی (Horia Hulubei) و شیمیدان فرانسوی ایوت کاوچوی (Yvette Cauchois) ادعا کردند که عنصر شماره ۹۳ جدول تناوبی را کشف کرده اند. اما با توجه به اینکه این عنصر در طبیعت در دسترس نبود، این ادعا نیز مورد انتقاد قرار گرفت.
در نهایت عنصر نپتونیم در سال ۱۹۴۰ میلادی، توسط فیزیکدانان امریکایی از دانشگاه کالیفرنیا، موسوم به ادوین مک میلان (Edwin Mattison McMillan) و فیلیپ آبلسون (Philip Hauge Abelson) کشف شد. آنها با استفاده از نوترون هایی با سرعت کم (در واقع به کمک شتاب دادن نوترون ها به روش سیکلوترون) یک هدف اورانیمی را بمباران کردند. بدین صورت پرتو های بتای غیر عادی نشر شد. این پرتو ها نشان دهنده ایزوتوپی جدید بودند. آبلسون ثابت کرد که مطمئنا یک عنصر جدید ساخته شده است. به عبارت دیگر، عنصر نپتونیم برای اولین بار به صورت مصنوعی ساخته شد. نخستین ترکیب نپتونیوم خالص، اکسید نپتونیم- ۲۳۷ در سال ۱۹۴۴ میلادی بدست آمد. نام این عنصر از نام سیاره نپتون گرفته شده است.
پیدایش و منابع عنصر شماره ۹۳ جدول تناوبی
همانطور که بیان شد، این عنصر در گروه عناصر کمیاب زمین قرار دارد. نپتونیوم در طبيعت به مقادير بسيار اندك در تمام سنگ های معدنی اورانیوم (پیچبلند) یافت می شود. دسترسی به نپتونیم و دیگر عناصر کمیاب در سال های اخیر بسیار پیشرفت کرده است. این فلز را می توان با کاهش فلورید نپتونیم (NpF۳) با باریم و یا استفاده از بخار لیتیوم در دمای ۱۲۰۰ درجه سانتیگراد تهیه نمود. این عنصر همچنین از رها شدن قدرت سوخت هسته ای در تهیه پلوتون (به عنوان یک فرآورده) بدست مي آيد. به عبارت دیگر می توان گفت که عنصر نپتونیوم يك محصول جانبي در رآكتور هايی محسوب می شود كه از عنصر اورانيم به عنوان ميله های سوختی خود بهره می برند. به بیان دیگر، این عنصر در پي بمباران نوترونی آن گرفته می شود.

ویژگی های فیزیکی و شیمیایی عنصر نپتونیم
عنصر نپتونیم، فلزی پرتوزا و رادیواکتیو است. این عنصر از عناصر سری اکتینید ها (بلوک- f) محسوب می شود. وجه تمايز عنصر نپتونيم با سایر عناصر در اين است كه نخستين عنصر فرا اكتينيدی است كه به صورت مصنوعی در آزمايشگاه توليد شده است. نپتونیوم اولین عنصر از سری آکتنید ها است که عدد اتمی بیشتر از عنصر اورانیم دارد. این عنصر به عنوان اولین ترانس اورانیم سری اکتنید ها کشف شده است. به بیان دیگر، از لحاظ شیمیایی عنصر نپتونیوم شبیه عنصر اورانیوم است.
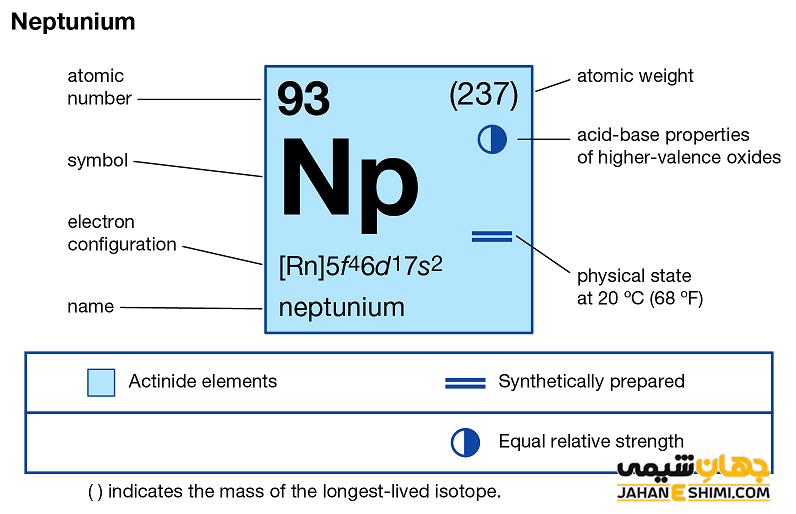
خصوصیات قابل توجه نپتونیم از ساختار اتمی آن ([۸۶Rn] 5f۴۶d۱۷s۲) ناشی می شود. همان طور که مشخص است، زیر لایه f در این عنصر در حال پر شدن است. این عنصر نیز همانند لانتانید ها و اکتینید ها و به واسطه آرایش الکترونی که دارد، در دسته فلزات واسطه داخلی قرار می گیرد. در واقع در این دسته از عناصر، الکترون های متمایز کننده در تراز های F(n-2) لایه ظرفیت که در واقع تراز های درونی اند قرار می گیرند. به همین دلیل، به عناصر واسطه داخلی معروف می باشند. این عناصر جزء عنصر های فلزات واسطه جدول تناوبی می باشند.فلزات واسطه قرار می گیرد. فلزات واسطه در حقیقت بین فلزات قلیایی خاکی (گروه دوم) و عناصر گروه بور در جدول تناوبی قرار گرفته اند. به عناصر واسطه، عناصر گروه B نیز گفته می شود.
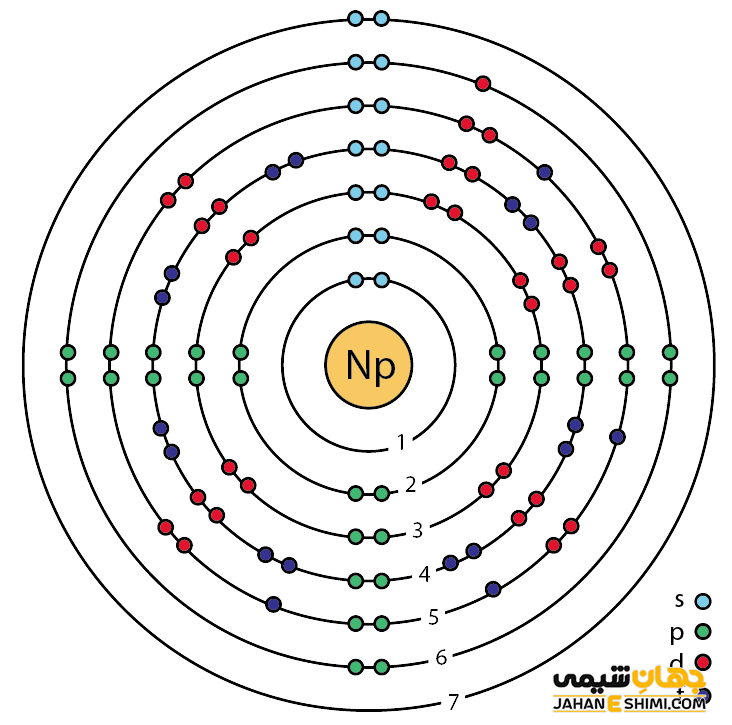
با توجه به آرایش الکترونی مشخص است که هفت الکترون در دورترین لایه الکترونی نپتونیم وجود دارد. پس می تواند در ترکیبات به صورت کاتیون های مختلف ظاهر شود. حالت اکسیداسیون آن بیشتر ۵+ است. از این رو می تواند در پنج پیوند کووالانسی شرکت کند.
خواص ویژه نپتونیوم
از نظر شیمیایی عنصر نپتونیوم دارای سه نوع ساختار شیمیایی مختلف است.
- نپتون آلفا، ساختار آن ارتورموبیک است. این ساختار چگالی برابر با ۲۰/۲۵ گرم بر سانتی متر مکعب دارد.
- نپتون بتا (بالای ۲۸۰ درجه سانتی گراد)، ساختار آن تتراگونال یا چهار وجهی است که چگالی ۱۹/۳۶ گرم بر سانتی متر مکعب دارد.
- نپتون گاما (بالای ۵۷۷ درجه سانتی گراد) که ساختار کوبیک یا مکعبی دارد. چگالی آن برابر با ۱۸/۰۰ گرم بر سانتی متر مکعب می باشد.
عنصر نپتونیم همچنین پنج حالت اکسیداسیونی به حالت محلول دارد. کاتیون سه بار مثبت یعنی Np+۳ (ارغوانی کمرنگ)، کاتیون چهار بار مثبت یعنی Np+۴ مشابه کاتیون عنصر Pm+۳ (زرد سبز)، کاتیون پنج بار مثبت یعنی NpO+۲ (سبز آبی)، کاتیون شش بار مثبت یعنی NpO۲+۲ (صورتی کمرنگ) و کاتیون هفت بار مثبت یعنی NpO+۳ (سبز تیره).

از دیگر ویژگی های عنصر رادیم می توان به موارد زیر اشاره کرد.
- حالت فیزیکی آن در دمای ۲۵ درجه سلسیوس و فشار ۱ اتمسفر به صورت جامد است.
- دمای ذوب و دمای جوش این عنصر به ترتیب ۶۳۷ و ۴۰۰۰ درجه سانتی گراد است.
- عنصر نپتونیم پارا مغناطیس است.
- ساختار بلوری آن به شکل اورتورومبیک (Simple Orthorhombic)است.
- این عنصر آلوتروپ ندارد.
- جرم اتمی نپتونیم برابر با ۲۳۷ g/mol است.
- چگالی آن نیز برابر با ۲۰.۲ g/cm۳ می باشد.
- شعاع اتمی آن نیز برابر با ۱۵۵ pm تخمین زده می شود.
- یون های نپتونیم معمولا اعدد اکسایش برابر با اعداد ۰، +۲، +۳، +۴، +۵، +۶ و +۷ دارند. در حقیقت یک اکسید آمفوتری محسوب می شود. اعداد اکسایش ۰ و +۵ متداول تر می باشند.
- اولین انرژی یونیزاسیون آن برابر با ۶۰۴.۵ kJ/mol است.
اکتینید ها
کلمه اکتینید (Actinide) به معنای شبیه اکتینیوم است که به طور کلی با نماد شیمیایی An نمایش داده می شود. همانطور که معلوم است، نام این سری از عناصر، از آکتینیوم گرفته شده است. بنابراین خواص شیمیایی این عناصر شبیه به عنصر اکتینیوم خواهد بود. اکتینید ها در واقع شامل ۱۵ عنصر با عدد های اتمی ۸۹ تا ۱۰۳ می باشند. گروه اکتینید ها در واقع با فلز اکتینیوم آغاز و به فلز لارنسیوم ختم می شود. در این دسته از عناصر، زیر لایه ۵ اف در حال پر شدن است. به دلیل کمبود جا در جدول و به منظور اینکه نظم و ترتیب جدول تناوبی عناصر بهم نخورد، این گروه از عناصر در یک ردیف ۱۴ تایی در پایین جدول قرار گرفته اند.
تمامی اکتینید ها به جز فلز اکتینیم جز بلوک f جدول هستند. عنصر اکتینیم جز بلوک d جدول تناوبی محسوب می شود، اما خواص آن شبیه به چهارده اکتینید دیگر است. لازم به ذکر است که با کشف نپتونيم مشخص شد، عناصر توریم، اورانیوم و نپتونیم می توانند سری جدیدی از عناصر خاک های کمیاب را تشکیل دهند. بنابراین برای متمایز شدن آنها از عناصر سری خاک های کمیاب قبلی که با نام عناصر لانتانید شناخته شده بودند، این سری جدید را عناصر اکتینید نام گذاری کردند.

خواص ویژه اکتینید ها
از عنصر چهارم این سری به بعد که به عناصر ترانس اورانیوم مشهورند، در طبیعت یافت نمی شوند. تمامی آنها هسته ناپایدار دارند، بنابراین جز عناصر پرتوزا و رادیواکتیو حساب می شوند. این عناصر، معمولا فلزاتی متراکم، نرم، انعطاف پذیر، چگالی بالا و الکتروپوزیتیو هستند. برخی از آنها با چاقو به راحتی برش می خورند. ممکن است آلوتروپ های زیادی تشکیل دهند. معمولا خاصیت پارامغناطیسی نشان می دهند. این فلزات در دمای اتاق جامد بوده و در هوا، خود به خودی آتش می گیرند. با هالوژن ها، کالکوژن ها و یا کربن (تشکیل ترکیبات اورگانو اکتینید) واکنش می دهند. همچنین با آب جوش و اسید های رقیق، گاز هیدروژن آزاد می نمایند. توجه کنید که برای مطالعه اکتینید ها، ساختار هسته عناصر نسبت به آرایش الکترونی آنها از اهمیت بیشتری برخوردار است.
ایزوتوپ های عنصر نپتونیم
همانطور که می دانید، ایزوتوپ های یک عنصر، در تعداد نوترون ها با یکدیگر تفاوت دارند. عنصر نپتونیم ایزوتوپ های فراوانی دارد. از آنجاییکه نپتونیوم، عنصری مصنوعی است، بنابراین ایزوتوپ پایدار ندارد. این عنصر به صورت مصنوعی و در رآکتور های هسته ای تولید می گردد. در نتیجه نمی توان برای آن جرم اتمی استاندارد تعریف کرد. بیست ایزوتوپ پرتوزا از عنصر نپتونیم شناسایی شده است. رادیوایزوتوپ ۲۳۷Np پایدار ترین ایزوتوپ نپتونیوم با نیمه عمر ۲٫۱۴ میلیون سال است. لازم به ذکر است که تمام ايزوتوپ هاي نپتونیوم از لحاظ شيميايي فوق العاده فعال می باشند. ایزوتوپ های رادیواکتیو این عنصر دارای جرم های اتمی در محدوده ۲۲۵ تا ۲۴۴ amu می باشند.
بعد از ایزوتوپ ۲۳۷Np، رادیو ایزوتوپ های ۲۳۶Np با نیمه عمر ۱۵۴۰۰۰ سال و ۲۳۵Np با نیمه عمر ۳۹۶/۱ روز هستند. بقیه ایزوتوپ های رادیو اکتیو آن، نیمه عمری کمتر از از ۴/۵ روز دارند. لازم به ذکر است که بیشتر آنها نیمه عمری کمتر از ۵۰ دقیقه دارند. علاوه بر آن، توریم دارای چهار حالت متا (m) نیز می باشد.

کاربرد های عنصر نپتونیم
عنصر نپتونیم خیلی به ندرت کاربردی خارج از پژوهش های علمی و تحقیقاتی دارد. از رادیو ایزوتوپ ۲۳۷Np به منظور تولید پلوتونیم- ۲۳۸ استفاده می شود. عنصر پلوتونیم- ۲۳۸ در ژنراتور هواپیما و همچنین چراغ های ناوبری زمینی مورد استفاده قرار می گیرد. این ایزوتوپ همچنین در تجهیزات ردیابی نوترونی (آشکارساز نوترونی) کاربرد دارد. به بیان دیگر می توان گفت که فرم تجاری این عنصر، ایزوتوپ رادیواکتیو ۲۳۷ می باشد.
ترکیبات عنصر نپتونیم
عنصر نپتونیم می تواند به راحتی با اکسیژن و هالوژن ها واکنش دهد. در نتیجه اکسید و هالید ها را تولید نماید. از جمله ترکیبات آن می توان به موارد زیر اشاره کرد.
- دی هیدرید نپتونیم (NpH۲)
- تری هیدرید نپتونیم (NpH۳)
- اکسید نپتونیم (NpO)
- دی اکسید نپتونیم (NpO۲)
- پنتا اکسید دی نپتونیم (Np۲O۵)
- اکتا اکسید تری نپتونیم (Np۳O۸)
- تری کلرید نپتونیم (NpCl۳)
- تترا کلرید نپتونیم (NpCl۴)
- پنتا کلرید نپتونیم (NpCl۵)
- هگزا کلرید نپتونیم (NpCl۶)
- تری فلوئورید نپتونیم (NpF۳)
- تترا فلوئورید نپتونیم (NpF۴)
- پنتا فلوئورید نپتونیم (NpF۵)
- هگزا فلوئورید نپتونیم (NpF۶)
- تری برمید نپتونیم (NpBr۳)
- تری یدید نپتونیم (NpCl۴)
- نپتونوسن (Np(C۸H۸)۲)
خطرات نپتونیوم بر روی سلامتی انسان
بخش زیادی از نپتونیمی که در بدن باقی مانده است، در استخوان ها نهشته می شود. مقداری از آن هم در کبد باقی می ماند. نپتونیم در واقع سبب افزایش تومور های استخوانی می شود. بنابراین از جمله عوارض احتمالی آن می توان به سرطان استخوان اشاره کرد. در مطالعات و تحقیقاتی مختلفی که بر روی جانوران آزمایشگاهی انجام شده است، مشخص می کند که غلظت نپتونیم در غده آدرنال بدن جانوران بالا می باشد. از طرفی دیگر، اندامی که دوز بالایی از نپتونیوم را دریافت می کنند مجاری گوارشی است. لازم به ذکر است که تا امروز هیچ اثر زیست محیطی منفی از عنصر نپتونیوم گزارش نشده است.




















