خواص عنصر رنیوم چیست؟ کاربرد و ویژگی رنیوم را می شناسید؟

عنصر رنیوم از عناصر شیمیایی جدول تناوبی مندلیف بوده و با نماد شیمیایی Re شناخته می شود. عدد اتمی عنصر رنیوم ۷۵ و عدد جرمی آن ۱۸۶.۲۰۵ است. خواص عنصر رنیوم موجب شده است تا در گروه ۷ و دوره ۶ از جدول تناوبی قرار بگیرد. از ویژگی عنصر رنیوم می توان به رنگ سفید نقره ای آن اشاره نمود. همچنین رنیم از عناصر سنگین بشمار می آید. عنصر رنیوم از فلزات واسطه جدول تناوبی بشمار می آید. کاربرد عنصر رنیوم در ساخت موتور های جت بسیار زیاد است. به طوری که ۷۰ درصد تولید عنصر رنیوم به موتور های جت اختصاص می یابد. از دیگر کاربرد عنصر رنیوم می توان به ساخت کاتالیزور اشاره کرد. ایزوتوپ عنصر رنیوم نیز شناخته شده و در ادامه بررسی خواهد شد. مدل اتمی بور برای عنصر رنیوم نیز می تواند به شناخت این ماده کمک نماید.
نشریه علمی جهان شیمی فیزیک به بررسی عناصر شیمیایی جدول تناوبی مندلیف پرداخته است. عناصری مانند: عنصر تانتال، عنصر هافنیم، عنصر لوتسیم، عنصر اربیم و… . در ادامه با بررسی کاربرد و خواص عنصر رنیوم با ما همراه باشید.
در باره تاریخچه عنصر رنیوم
مندلیف در سال ۱۸۷۱ وجود دو عنصر شبیه به منگنز در جدول تناوبی را پیش بینی نمود. امروزه این دو عنصر تکنسیم و رنیوم نامیده می شوند. آیدا و والتر نوداک در سال ۱۹۲۲ آزمایشاتی بر روی سنگ های معدن پلاتین انجام دادند. آن ها به دلیل هزینه زیاد این آزمایشات مجبور به تغییر سنگ معدن انتخابی شدند.
در نهایت نوداک ها ادعا کردند که با انجام آزمایش سنگ معدن های مختلف با کمک دستگاه اسپکتروسکوپ این دو عنصر شبیه به منگنز را یافتهاند. لازم به ذکر است اسپکتروسکوپ دستگاهی است که با اشعه X و فرکانس های حاصل از آن، عناصر شناسایی میشوند. درنهایت آن ها نام این دو عنصر را ماسوریوم و رنیوم گذاشتند.
البته نوداک ها در مناظره با دانشمندی آلمانی نتوانستند دلایل قانع کننده ای در مورد ماسوریوم به وی ارائه دهند. اما دلایل آن ها برای اثبات خواص عنصر رنیوم کافی بود. بدین ترتیب عنصر رنیوم به نام عنصر شماره ۷۵ جدول تناوبی شناخته شد. جالب است بدانید که کشف عنصر رنیوم، آخرین عنصر موجود در طبیعت بود.
منابع
عنصر رنیوم از کمیاب ترین عناصر زمین است. فراوانی این ماده در پوسته زمین، یک در میلیارد تخمین خورده است. حتی کمتر از ۱۰ گرم رنیوم در هر تن از غنی ترین سنگ معدن های رنیوم در کشور قزاقستان وجود دارد. این عنصر در بین تمامی عناصر بالا ترین نقطه جوش را داراست. تولید این فلز از معدن رنیوم در سراسر جهان سالانه ۵۰ تا ۶۰ تن برآورد شده است. ۵۰٪ این ماده از بزرگ ترین معادن مس پورفیری شیلی به دست می آید.
لازم به ذکر است که عنصر رنیوم به صورت فلز آزاد و بدون ترکیب با سایر مواد در طبیعت وجود ندارد. درواقع هیچ سنگ معدنی خالص از این ماده در طبیعت یافته نمی شود. سنگ معدن گادولینیت و مولیبدنیت ممکن است حاوی کمی از این ماده باشند. تولید جهانی سالانه این فلز در حال حاضر حدود ۵ تن و ذخایر تخمینی رنیوم ۳۵۰۰ تن است. عمده ذخایر این فلز در ایالات متحده آمریکا، روسیه و شیلی یافت می شود.
تولید رنیوم در جهان
رنیم از دسته فلزات واسطه است. خواص عنصر رنیوم از نظر ظاهری به منگنز و تکنسیوم شباهت دارد. تولید رنیم این از طریق استخراج و پالایش سنگ های معدنی مس و مولیبدن ایجاد میشود. تقریبا تمام رنیوم تولید شده توسط استخراج (و نه بازیافت) از طریق محصول جانبی استخراج مس است. نام این عنصر که در سال ۱۹۲۵ کشف شد برگرفته از رود راین در اروپای غربی است.
ویژگی عنصر رنیوم عنصر شماره ۷۵ جدول تناوبی عناصر
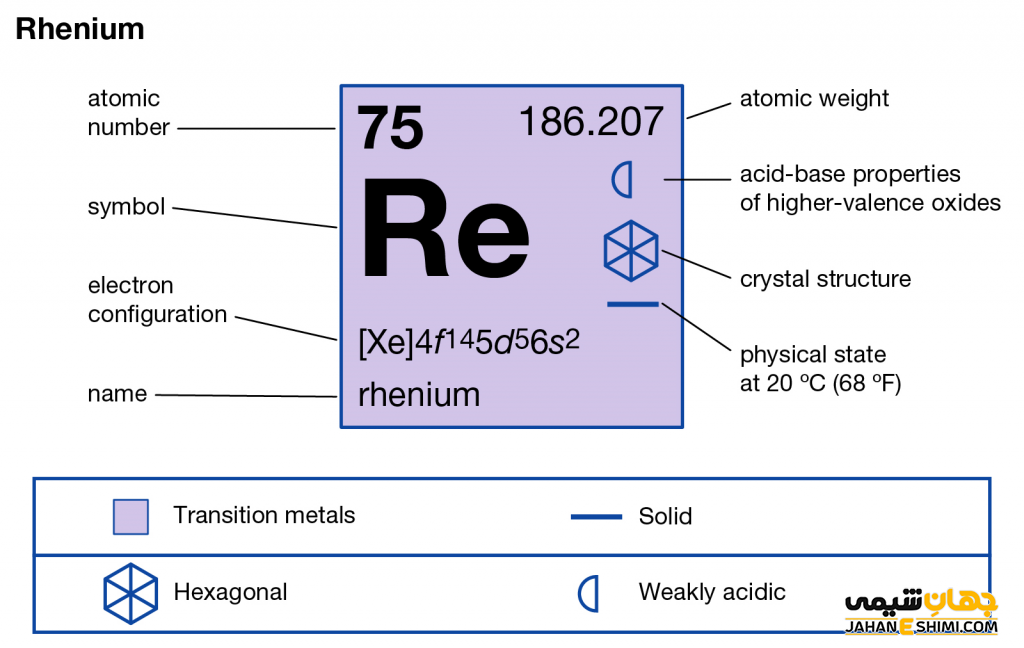
- نشان (نماد) شیمیایی: Re
- عدد اتمی: ۷۵
- جرم اتمی (عدد جرمی): ۱۸۶٫۲۰۷
- نقطه ذوب : ۳۱۸۶ درجه سانتی گراد
- نقطه جوش: ۵۵۹۶ درجه سانتی گراد
- گروه: ۷
- تناوب: ۶
- شعاع اتمی: ۱۳۷ pm
- ظرفیت : ۶
- رنگ : سفید خاکستری
- حالت استاندارد (شرایط STP): جامد
- نام گروه : عناصر واسطه
- آرایش الکترونی: [Xe] 4f۱۴ ۵d۵ ۶s۲
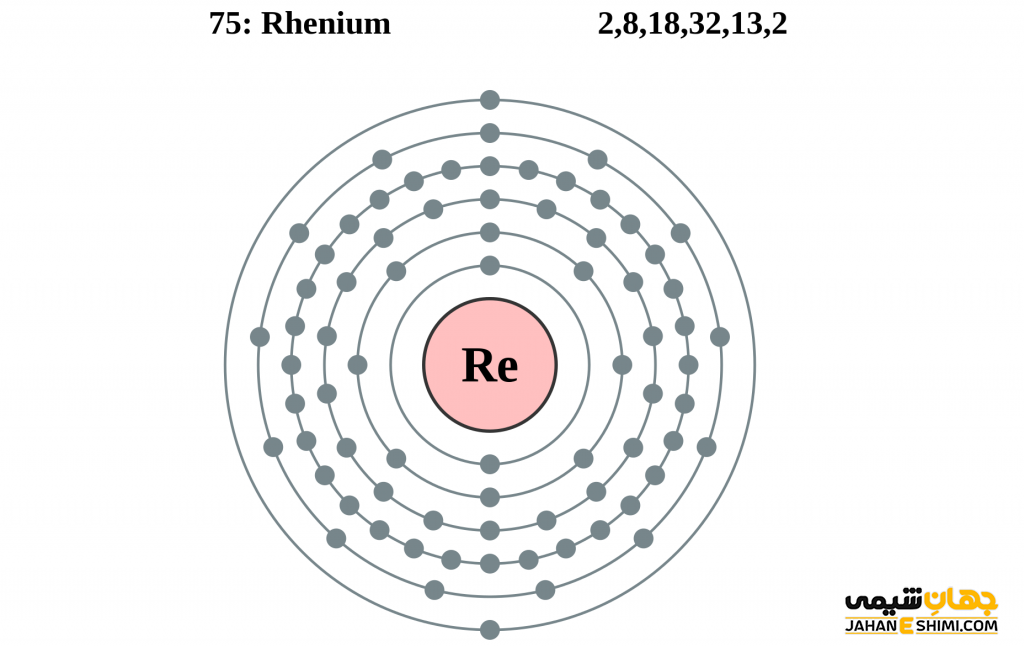
- لایه الکترونی: ۲, ۸, ۱۸, ۳۲, ۱۳, ۲
- چگالی: ۲۱.۰۲ گرم بر سانتی متر مکعب
خواص عنصر رنیوم
از خواص عنصر رنیوم می توان به این اشاره کرد که فلزی درخشان و سفید مایل به نقره ای است. عنصر رنیوم عنصر شماره ۷۵ جدول تناوبی عناصر است. این عنصر بالاترین نقطه ذوب را در میان عناصر به جز تنگستن و کربن داراست. بعد از عناصری نظیر پلاتین، ایریدیوم و اوسمیوم بالاترین چگالی متعلق به رنیم است. حالت های اکسیداسیون برای این عنصر عبارتند از:
-۱,+۱,+۲,+۳,+۴,+۵,+۶,+۷ که حالت های +۷,+۶+۴+۲ و -۱ از بقیه محتمل تر هستند.
پودر رنیوم به صورت تجاری در دسترس است. این ماده با اعمال فشار در خلأ یا هوای هیدروژنی محکم می شود. بدین صورت شکل فشرده ای از این ماده به وجود آمده که ۹۰% چگالی فلز را داراست.
جالب است بدانید عنصر رنیوم در هنگام حرارت دادن بسیار رسانا می شود. همچنین به آسانی خم شده و به شکل مارپیچ و یا رول در می آید. آلیاژ رنیوم-مولیبدن از آلیاژهای بسیار رسانا (ابر رسانا) شناخته می شود. برای شناخت بیشتر خواص عنصر رنیم می توانید به مدل اتمی بور برای عنصر رنیوم مراجعه نمایید.
فلزات واسطه
عناصر واسطه به عناصری گفته می شود که اوربیتال فرعی d آن ها به صورت جزئی پر شده باشد. و یا اینکه از طریق آرایش اوربیتالی ناقص به صورت کاتیون وجود داشته باشند. درواقع هر عنصر از بلوک d جدول تناوبی به عنوان عناصر واسطه شناخته می شوند. فلزات واسطه گروه ۳ تا ۱۲ جدول تناوبی عناصر را تشکیل می دهند. عناصر بلوک f شامل لانتانید ها و اکتینید ها نیز در طبقه بندی فلزات واسطه قرار میگیرند. فلزات واسطه داخلی نامی است که بر لانتانیدها و اکتانیدها نهادهاند. فلزات واسطه در میان فلزات قلیایی خاکی و عناصر گروه بور قرار دارند. عناصر دسته d، چگالی، نقطه ذوب و نقطه جوش بالایی دارند. تمام فلزات واسطه رسانای خوب جریان الکتریسیته هستند. این خواص به خاطر پیوند فلزی و جذب الکترون های زیر لایه d است. این موارد به افزایش تعداد الکترون های اشتراکی و چسبندگی مولکول ها منجر شده است.
خواص عناصر واسطه
این عناصر ترکیبات رنگی تشکیل می دهند که علت آن انتقالات الکترونی d-d است. علت رنگی بودن برخی ترکیبات فلزات واسطه، در حالت گذار الکترونی است. این حالات دو اصل مهم را شامل می شود. انتقال بار و حالت گذار اوربیتال های d.
اختلاف انرژی در حالت های مختلف عدد اکسایش پایین است. بنابراین ترکیباتی با اعداد اکسایش متفاوت تشکیل می شود.
بسیاری از ترکیبات پارامغناطیس به دلیل حضور الکترون های جفت نشده تشکیل می شوند.
در پیوند با لیگاند ها، بیشتر فلزات واسطه موجب تشکیل کمپلکسهای فلزی زیادی میشوند.
یکی از شاخصه های مهم عناصر واسطه اعداد اکسایش متفاوت است.
عناصر واسطه و ترکیباتشان بر مبنای فعالیت های کاتالیستی همگن و ناهمگن نیز شناخته میشوند.
ایزوتوپ عنصر رنیوم
عنصر رنیوم بهصورت طبیعی بوجود آمده و تنها یک ایزوتوپ پایدار و یک ایزوتوپ رادیو اکتیو (رادیو ایزوتوپ) دارد. رادیو ایزوتوپ عنصر رنیوم از نیمه عمر بالایی برخوردار است. اما لازم به ذکر است که برای این ماده ۲۶ ایزوتوپ ناپایدار نیز شناخته شده است.
| نیمه عمر | ایزوتوپ |
| ۲.۶۷ روز | Re-182 |
| ۱۲.۷ ساعت | Re-182m |
| ۷۰ روز | Re-183 |
| ۳۸ روز | Re-184 |
| ۱۶۵ روز | Re-184m |
| پایدار | Re-185 |
| ۳.۷۷ روز | Re-186 |
| ۱۰E4.1 سال | Re-187 |
| ۱۶.۹۴ ساعت | Re-188 |
کاربرد ایزوتوپ رنیوم
خواص رادیو دارویی رنیوم دارای برچسب Rhenium-188 و کاربرد های بالینی فعلی این ماده در آنکولوژی مورد بررسی قرار گرفته است.
۱۸۸Re یک رادیو ایزوتوپ پرتوزا بتا با نیمه عمر فیزیکی کوتاه ۱۶.۹ ساعت است. ۱۸۸Re یک کاندید بسیار خوب برای کاربرد در درمان های پزشکی هسته ای است.
میزان انتشار بتا زیاد این مواد برای نفوذ و از بین بردن هدفمند بافت های غیر طبیعی کافی است. این ویژگی های کلیدی ۱۸۸Re را به عنوان یک رادیو ایزوتوپ درمانی مهم برای استفاده های بالینی معمول معرفی می کند.
دارو های رادیواکتیو ۱۸۸Re در بیماران برای درمان سرطان بررسی شده است. رنیوم ۱۸۸ در مقایسه با رادیو ایزوتوپ های درمانی گران قیمت و یا با دسترسی کمتر گزینه ای مقرون به صرفه برای استفاده بالینی هستند.
کاربرد عنصر رنیوم
کاربرد عنصر رنیوم در ساخت کاتالیزور پلاتین-رنیوم کاربرد دارد. این کاتالیزور در ساخت بنزین سوپر و بدون سرب کاربرد دارد.
آلیاژ عنصر رنیوم برای قطعات مختلف موتور هواپیما کاربرد دارد.
کاربرد عنصر رنیوم بهصورت Filament در طیف سنج جرمی و اندازه گیری های یونی صورت می پذیرد.
کاربرد این ماده برای القا خواص مفید به آلیاژ صورت می گیرد. از این ماده بهعنوان ماده اضافه شونده به تنگستن و آلیاژ های مولیبدنی استفاده میشود.
از ویژگی و خواص عنصر رنیوم در سوپرآلیاژ ها به عنوان یک جزء مهم استفاده می شود. از این عنصر در ساخت موتورهای توربین نیز استفاده می شود و این کاربرد اصلی این عنصر است.
کاتالیزور ها رنیومی در مقابل واکنش های شیمیایی بسیار مقاوم هستند. بنابراین در واکنش های هیدروژنی استفاده می شوند.
از خواص عنصر رنیوم به عنوان ماده مخصوص برای اتصالات الکترونیکی استفاده می شود.
جهت اندازه گیری دماهای بالا تا ۲۲۰۰ درجه سانتیگراد از ترموکوپل هایی استفاده می شود که آلیاژ تنگستن و رنیوم دارند.
از سیم رنیوم نیز می توان در ساخت لامپ های فلاش دوربین عکاسی استفاده نمود.
قیمت رنیوم
عنصر رنیوم به دلیل کمیاب بودنش از گران ترین فلزات است. تنها طلا و فلزات گروه پلاتین هستند که از این فلز گرانتر هستند. قیمت رنیوم طی سال های ۲۰۰۳ تا ۲۰۰۶ هزار تا دو هزار دلار برای هر کیلوگرم بود. در سال ۲۰۱۱ میانگین قیمت این فلز به ۴۵۷۵ دلار برای هر کیلوگرم رسید. کاربرد این فلز در ساخت جت های نظامی و موتور موشک ها منجر به اهمیت استراتژیکی این ماده نیز شده است.
تاثیر خواص عنصر رنیوم بر سلامتی
اطلاعات ناچیزی در مورد سمیت رنیوم در دست است. تحریک چشم و پوست از اثرات این ماده بر سلامتی است. این عنصر در غلظت های بالا می تواند منجر به سوختگی گردد.
بلع این ماده شیمیایی تحریک دستگاه گوارش را منجر می شود. استنشاق رنیوم باعث تحریک دستگاه تنفسی خواهد شد. بخارات این ماده نیز سرگیجه و خفگی را ایجاد می کند.
چیزی در مورد نحوه رفتار این ماده در خاک، گیاهان و حیوانات مشخص نیست. زیرا عنصر رنیوم در محیط زیست بسیار کم است. هیچ موردی از آلودگی نمک های رنیوم از معدن یا صنعت وجود ندارد. اطلاعات خاصی هم در مورد سمیت محیطی رنیم ثبت نشده است.
سخن آخر
جهان هستی از عناصر مختلفی ساخته شده است. بدون عناصر شیمیایی جهان نمی توانست شکل بگیرد. بنابراین شناخت عناصر شیمیایی یکی از ملزومات علم است. عناصر شیمیایی در جدولی به نام جدول تناوبی مندلیف مرتب شده اند. درواقع در جدول تناوبی مندلیف عناصر گوناگونی جای گرفته اند. عناصر موجود در جدول تناوبی از لحاظ خواص فیزیکی و شیمیایی با یکدیگر تفاوت هایی دارند. وجود همین تفاوت هاست که منجر به خواص متفاوت آن ها شده است. ویژگی و خواص متفاوت عناصر، کاربرد متنوع آن ها به وجود آورده است.

اغلب عناصری که در یک گروه از جدول تناوبی قرار دارند ویژگی های شیمیایی شبیه به هم نیز دارند. برای شناخت جایگاه این عناصر می توان به جدول تناوبی مندلیف مراجعه نمود. با نگاه به جدول تناوبی مشاهده می شود که تمام عناصر جایگاه مخصوص به خود را دارند. در واقع عناصر در گروه ها و تناوب هایی چیده شده اند. کاربرد مختلف عناصر در صنایع و سلامت و پزشکی و کشاورزی و سایر کاربرد ها تنها با شناخت صحیح و کامل عناصر امکان پذیر خواهد بود. یادمان باشد توسعه بیشتر علم به توسعه و پیشرفت بیشتر جوامع انسانی می انجامد.
عناصر جدول تناوبی حالات مختلفی می توانند داشته باشند؛ که بستگی به خواص هر عنصر دارد. جامد، مایع، گاز، حالت های مختلف این عناصر است. برخی از عناصر جدول فلز و برخی نافلز و برخی از عناصر نیز شبه فلز هستند.
ارزش والای شیمی بر صنعت و اهمیت عناصر در زندگی بشر منجر شد تا نشریه علمی جهان شیمی فیزیک به توضیح و بررسی عناصر بپردازد. بنابراین برای آشنایی با خواص و کاربرد و تاریخچه تمام عناصر شیمیایی می توانید به سایت نشریه علمی جهان شیمی فیزیک مراجعه کرده و اطلاعات خود را گسترش دهید.



















