
عنصر آنتیموان (Antimony) با نماد شیمیایی Sb، یکی از عناصر شیمیایی جدول مندلیف است که عدد اتمی آن ۵۱ می باشد. این عنصر در حقیقت پنجاه و یکمین عنصر از جدول تناوبی بوده که در گروه XV و دوره پنجم جدول تناوبی قرار دارد. در واقع عنصر آنتیموان یک شبه فلز بسیار شکننده و به رنگ سفید مایل به آبی و از عناصر گروه نیتروژن است. این فلز با عناصر نیتروژن (N)، فسفر (P)، آرسنیک (As)، بیسموت (Bi) و مسکوویم (Mc)، در گروه پانزده یا گروه پنج اصلی جدول تناوبی قرار گرفته است. در ادامه این مقاله در نشریه جهان شیمی فیزیک به بررسی عنصر آنتیموان پرداخته می شود. لطفا با ما همراه باشید.
تاریخچه کشف عنصر آنتیموان
آنتیموان از گذشته های بسیار دور شناخته شده بود. در حقیقت مصریان باستان، از پودر آنتیموان برای آرایش چشم های خود استفاده می کردند. کلمه آنتیموان از واژه یونانی anti-monos به معنای غیر تنها (فلزی که به تنهایی یافت نمی شود) گرفته شده است. این عنصر در متون کهن فارسی به نام های روی سخته و یا روی سخته مصری نامگذاری شده است. در اوایل قرن ۱۷ میلادی به عنوان یک فلز شناسایی شد. برای نخستین بار شیمیدان فرانسوی یعنی نیکلاس لمری، آنتیموان و ترکیبات آن را به صورت علمی بررسی کرد. وی نتیجه تحقیقات خود را در سال ۱۷۰۷ میلادی منتشر کرد.

پیدایش و منابع عنصر شماره ۵۱ جدول تناوبی
عنصر آنتیموان گاهی اوقات به شکل آزاد در طبیعت یافت می شود، در صورتیکه به صورت عمده از کانی های زیبای استیبنایت (Sb۲S۳) و والنتینایت (Sb۲O۳) استخراج می گردد. همانطور که مشخص است، کانی هایی که منابع اصلی این عنصر محسوب می شوند در واقع سولفید و اکسیدی از آن می باشند. از جمله کانی های دیگری که تولید انتیموان از آنها ارزش اقتصادی داشته باشد می توان به کرمزیت (Sb۲S۲O)، تتراهدریت ارگانیفرس ((Cu,Fe)۱۲Sb۴S۱۳)، لیوینگستونیت (HgSb۴S۷) و جامسونیت (Pb۴FeSb۶S۱۴) اشاره کرد. به علاوه، مقادیر کمی از انتیموان نیز می تواند از فرآیند تولید مس و سرب بازیافت شود.

آنتیموان به دو شکل در طبیعت وجود دارد. یک فرم، فلزی است که روشن، نقره ای، سخت و شکننده می باشد. در حالیکه فرم دوم آن یک پودر غیر فلزی خاکستری رنگ است که در هوای خشک پایدار می باشد. در شکل زیر کشور های اول تولید کننده این عنصر آورده شده است.

ویژگی های فیزیکی و شیمیایی عنصر آنتیموان
عنصر آنتیموان، بسیار شکننده، گداز پذیر و بلوری است که بلافاصله پوسته پوسته می شود. خصوصیات قابل توجه آنتیموان از ساختار اتمی آن ([۳۶Kr] 4d۱۰۵s۲۵p۳) ناشی می شود. همانطور که مشخص است، اوربیتال p لایه آخر در این عنصر در حال پر شدن است. این عنصر دارای سه اوربیتال نیمه پر در اوربیتال p خود است. از این رو می تواند در سه پیوند کووالانسی شرکت کند. پس حالت های اکسیداسیون +۳ و -۳ را خواهد داشت. همچنین با توجه به آرایش الکترونی آن مشخص است که پنج الکترون در دورترین لایه الکترونی آنتیموان وجود دارد.

توجه داشته باشید که آنتیموان یک عنصر شیمیایی نیمه فلزی (Semimetallic) است. در واقع از نظر خصوصیات فیزیکی و ظاهری شبیه فلزت است. در حالیکه از لحاظ شیمیایی مانند فلزات واکنش نمی دهد. این شبه فلز دارای خاصیت هدایت الکتریکی و حرارتی ضعیفی است. همچنین در دمای کم تبخیر می گردد.
آنتیموان در هوای خشک پایدار است، اما بر روی شعله با نور آبی رنگ درخشانی خیلی سریع می سوزد. در این صورت مقادیر بسیار زیادی گاز های سفید رنگ (تری اکسید آنتیموان) ایجاد می کند. به بیان دیگر، آنتیموان فلزی در شرایط عادی در دمای اتاق تحت تاثیر هوا و یا رطوبت قرار نمی گیرد. اما دقت داشته باشید که اگر هوا مرطوب باشد، به تدریج می تواند اکسید شود. از طرفی دیگر، به وسیله اسید های رقیق یا قلیا مورد حمله قرار نمی گیرد. در حالیکه می تواند مورد حمله اکسید کننده های قویتر، گوگرد و هالوژن ها قرار گیرد. همچنین در صورت گرم شدن می تواند با اکسیژن، واکنش داده و تری اکسید آنتیموان (Sb۲O۳) را تولید کند. این اکسید هم در اسید ها و هم در مواد قلیایی محلول می باشد.
عنصر شماره ۵۱ جدول تناوبی می تواند به عنوان یک ماده اکسید کننده عمل نماید، در نتیجه با بسیاری از فلزات واکنش می دهد. در این صورت آنتی مونیدهایی (Antimonides)تشکیل می شوند که تا حدودی فلزی اند، اما به طور کلی شبیه آرسنید ها، نیترید ها و فسفید ها می باشد. نکته قابل توجه درباره آنتیموان و تعدادی از آلیاژ های آن اینست که در اثر خنک شدن می توانند منبسط شوند. اگر شکل مذاب آن به آرامی خنک شود، در یک سلول مثلثی شکل می گیرد. شکل های قابل دسترس آن معمولا به صورت شمش، قطعات خرد شده، ریز دانه، گلوله، بلور های مجزا، قالب های ریخته شده و پودر است. از دیگر ویژگی های عنصر آنتیموان می توان به موارد زیر اشاره کرد.

- حالت فیزیکی آن در دمای ۲۵ درجه سلسیوس و فشار ۱ اتمسفر به صورت جامد است.
- دمای ذوب و دمای جوش این عنصر به ترتیب ۶۳۰.۶۳ و ۱۵۸۷ درجه سانتی گراد است.
- عنصر آنتیموان دیا مغناطیس است.
- ساختار بلوری آن به شکل شش گوشه یا هگزاگونال (Hexagonal)است.
- این عنصر چهار آلوتروپ دارد. این آلوتروپ ها عبارتند از : آنتیموان آبی- سفید (شکل فلزی پایدار)، آنتیموان زرد، آنتیموان سیاه و آنتیموان انفجاری.
- جرم اتمی آنتیموان برابر با ۱۲۱.۷۶ g/mol است.
- چگالی آن نیز برابر با ۶.۶۹۷ g/cm۳ می باشد.
- شعاع اتمی آن نیز برابر با ۱۳۳ pm می باشد.
- یون های آنتیموان معمولا عدد اکسایش برابر با اعداد -۱، -۲، -۳، ۰، +۱،+۲ ، +۳، +۴ و +۵ دارند. در حقیقت یک اکسید آمفوتری محسوب می شود. اعداد اکسایش -۳، ۰، +۳، و +۵ متداول تر می باشند.
- اولین انرژی یونیزاسیون آن برابر با ۸۳۴ kJ/mol است.

شبه فلز ها
شبه فلز یا فلزوار (Metalloid) به عناصری گفته می شود که خواص آنها میان فلزات و نافلزات است. به طور کلی می توان گفت که خواص فیزیکی فلزوار ها بیشتر شبیه به فلزات، اما رفتار شمیایی آنها مثل نافلزات است. این دسته از عناصر شیمیایی، سطح صیقلی و براقی دارند. به علاوه، در اثر ضربه خرد می شوند. در نتیجه می شکنند، پس چکش خوار نیستند. به عبارت دیگر، شبه فلزات جامد هایی شکننده با ظاهری فلزی می باشند. این دسته عناصر تمایل دارند که در طی واکنش با سایر اتم ها، الکترون های خود را به اشتراک بگذارند.
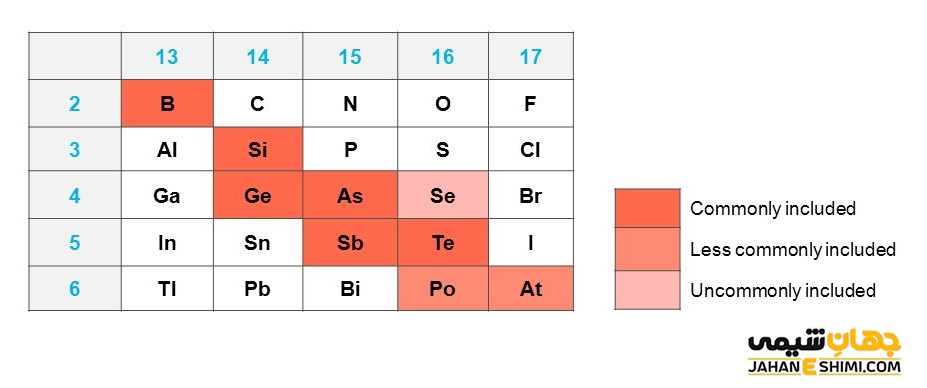
از دیگر خواص آنها اینست که بیشتر نیمه رسانا بوده و رسانایی گرمایی متوسطی نیز دارند. برخی از آنها مانند آرسنیک و آنتیموان، الکتریسیته را مانند فلزات هدایت می کنند. همچنین دارای اکسید های آمفوتری یا اسیدی ضعیف می باشند. این عناصر بیشتر به صورت ترکیب وجود دارند. شش شبه فلز شناخته شده عبارتند از : عناصر بور، سیلیکون، ژرمانیوم، آرسنیک، آنتیموان و تلوریوم.
ایزوتوپ های عنصر آنتیموان
همانطور که می دانید، ایزوتوپ های یک عنصر، در تعداد نوترون ها با یکدیگر تفاوت دارند. عنصر آنتیموان ایزوتوپ های فراوانی دارد. آنتیموانی که در طبیعت وجود دارد دارای دو ایزوتوپ پایدار ۱۲۳Sb (42.79 %) و ۱۲۱Sb (57.21 %) می باشد. علاوه بر آن، ۳۵ ایزوتوپ پرتوزای آنتیموان نیز شناخته شده است. پایدارترین رادیوایزوتوپ آنتیموان ۱۲۵Sb با نیمه عمر ۲/۷۵ سال است. ایزوتوپ های رادیواکتیو این عنصر دارای جرم های ۱۲۰ تا ۱۳۲ می باشند، که اغلب به شکل مصنوعی تولید می شوند. در جدول زیر نیمه عمر تعدادی از ایزوتوپ های رادیواکتیو آن را مشاهده می کنید.
| ۲/۸ ساعت | Sb-117 |
| ۳۸/۱ ساعت | Sb-119 |
| ۱۵/۸۹ دقیقه | Sb-120 |
| ۲/۷ روز | Sb-122 |
| ۶۰/۲ روز | Sb-124 |
| ۲/۷۵ سال | Sb-125 |
| ۱۲/۴ روز | Sb-126 |
| ۱۹ دقیقه | Sb-126m |
| ۳/۸۴ روز | Sb-127 |
| ۴/۴ ساعت | Sb-129 |
کاربرد های عنصر آنتیموان
لازم به ذکر است که حدود نیمی از آنتیموان تولیدی در کارهای متالورژی مصرف می شود. در واقع مهمترین کاربرد آن در تولید آلیاژ ها است. همانطور که بیان شد بعضی از آلیاژ های آنتیموان در طی فرآیند انجماد منبسط می شوند، پس به عنوان یک فلز ریختگی ارزشمند خواهد بود. در واقع، انبساط آلیاژ باعث می شود که فلز آنتیموان شکاف های کوچک در قالب های ریخته گری را پر کند. همچنین وجود انتیموان در آلیاژ هایی که دارای سرب و یا مقادیر کمی قلع باشند، سختی و مقاومت مکانیکی آلیاژ را افزایش می دهد. آلیاژ های تشکیل شده را می توان به طور گسترده در صفحات باتری اتومبیل، فلزات با اصطکاک کم ،گلوله ها، پوشش کابل ها، به عنوان سخت کننده سرب در خازن ها و تجهیزات شیمیایی مثل مخازن و لوله ها بکار برد.
عنصر شماره ۵۱ جدول تناوبی همچنین آلیاژ های ضد اصطکاکی به نام بابیت تشکیل می دهد. این آلیاژ در اجزای یاتاقان های ماشین ها کاربرد دارند. از طرفی دیگر، به همراه عنصر قلع، آلیاژ هایی همچون بریتانیا و پیوتر را تشکیل می دهد که برای ظروف بکار می روند. از آنتیموان همچنین به عنوان آلیاژ لحیم کاری بهره می برند. از انواع بسیار خالص و ویژه آن در فناوری نیمه هادی برای تهیه دیود ها و ردیاب های مادون قرمز استفاده می شود. از آنجاییکه آنتیموان یک رسانای ضعیف برای گرما و الکتریسیته می باشد، بنابراین جز سازنده مناسبی در مواد نیمه رسانای میکروالکترونیک ها خواهد بود.

ترکیبات انتیموان (مثلا اکسید، سولفید، آنتیمونات سدیم و تری کلرید آنتیموان) برای ساخت مواد ضد حریق، رنگ سازی، تولید پلاستیک و لاستیک، مینای دندان، لعاب سرامیک، کاغذ، شیشه، منسوجات و وسایل الکترونیک و سفالگری بکار می رود. تری اکسید آنتیموان یکی از مهمترین ترکیبات آنتیموان است. این ترکیب بیشتر برای کاربرد های ضد شعله و همچنین در تنظیمات واپسگر آتش کاربرد دارد. کاربرد های اصلی این نوع بازدارنده های آتش، در مواردی مانند لباس کودکان، مبلمان، اسباب بازی ها، هواپیما، روکش صندلی های اتومبیل و روکش موتور هواپیما های سبک است. علاوه بر آن، ترکیب پتاسیم آنتیموان تارتارات (Tartar Emetic) که در حقیقت یک نمک آلی آنتیموان است، در صنایع نساجی و پزشکی کاربرد دارد. در نساجی برای کمک به اتصال بعضی از رنگ ها به پارچه و در پزشکی به عنوان داروی خلط آور و تهوع آور بکار برده می شود.
از دیگر کاربرد های آنتیموان می توان به ساخت سقف های کاذب، تزئینات داخلی منازل، سپر های رادیواکتیو (در مقابل اشعه گاما و ایکس مقاومند)، صنایع مهمات و اسلحه سازی، لنز های دوربین، دستگاه های فتوکپی، دستگاه های تلویزیون، فلز ویژه حروف چاپ، تولید دیسک های دیجیتالی (DVD) و فولاد های مغناطیسی را نام برد. یک کاربرد مهم دیگر آن استفاده به عنوان یک تثبیت کننده و کاتالیزور جهت تولید پلی اتیلن ترفتالات می باشد. همچنین به عنوان یک عامل ریز کننده به منظور از بین بردن حباب های میکروسکوپی در شیشه ها (به ویژه صفحات تلوزیون) است. لازم به ذکر است که در زیست شناسی و پزشکی کاربرد های کمی برای این عنصر گزارش شده است. به عنوان مثال آنتیموان و ترکیباتش در چندین داروی دامپزشکی بکار رفته است.
ترکیبات عنصر آنتیموان
اکسید آنتیموان یکی از مهمترین ترکیبات کاربردی فلز آنتیموان است. این فلز همچنین می تواند به راحتی با هالوژن ها و گوگرد نیز واکنش دهد و در نتیجه هالید ها و سولفید تولید نماید. از دیگر ترکیبات آن می توان به موارد زیر اشاره کرد.
- آنتیموان تری اکسید (Sb۲O۳)
- پنتاکسید آنتیموان (Sb۲O۵)
- سروانتیت یا آنتیموان تروکسید (Sb۲O۴)
- آنتیموان پنتاسولفید (S۵Sb۲)
- آنتیموان تری فلورید (SbF۳)
- آنتیموان تریبرمید (SbBr۳)
- آنتیموان تری کلرید (SbCl۳)
- آنتیموان ترییدید (SbI۳)
- آنتیموان پنتا فلورید (SbF۵)
- آنتیموان پنتا کلرید (SbCl۵)
- آنتیموان هیدرید (SbH۳)
- استات آنتیموان(III) (C۶H۹O۶Sb)
- فلوئورو آنتیمونیک اسید (HSbF۶)
- آلگاروت (SbOCl)
- تیو آنیمونیات سدیم (Na۳SbS۴·۹H۲O)
- تریسلنید آنتیموان (Sb۲Se۳)
- پتاسیم آنتیمونیل تارترات (K۲Sb۲(C۴H۲O۶)۲ ۳H۲O)
- آنتیموان آنتیمونید (InSb)
- آنتیموان سولفات (Sb۲(SO۴)۳)

خطرات آنتیموان بر روی سلامتی انسان
آنتیموان خالص و ترکیباتش بسیار سمی هستند. بنابراین در هنگام کار با آنها باید احتیاط کرد. افرادی که با آنتیموان کار می کنند، به دلیل تنفس گرد و غبار آن عوارضی را نشان می دهند. همچنین از طریق تماس پوست با خاک، تنفس هوا، آب و مواد غذایی که حاوی این عنصر هستند، آنتیموان وارد بدن انسان می شود. در این صورت اثرات منفی زیادی بر روی سلامتی خواهد داشت. به عنوان مثال، قرار گرفتن به مدت طولانی در معرض غلظت زیاد این عنصر می تواند باعث تحریک چشم ها، پوست و ریه ها گردد. حتی می تواند باعث بیماری هایی همچون بیماری های ریوی، مشکلات قلبی، اسهال، استفراغ شدید و زخم معده گردد. لازم به ذکر است که هنوز به طور دقیق ثابت نشده است که آیا آنتیموان می تواند باعث سرطان یا نارسایی تولید مثل (ناتوانی جنسی) شود یا خیر.
قیمت جهانی آنتیموان
آنتیموان یک عنصر شیمیایی است که می تواند فلزی یا غیرفلزی باشد. فرم فلزی یک ماده نقره ای روشن است که شکننده است. پودر خاکستری شکل غیرفلزی آنتیموان است. در هوای خشک، آنتیموان عنصری پایدار است که نسبت به اسیدها و قلیاها بی اثر است. آنتیموان با سرد شدن منبسط می شود و رسانای ناکارآمد الکتریسیته و گرما است. آنتیموان یکی از قدیمی ترین عناصر شناخته شده برای بشر است که از ۴۰۰۰ سال قبل از میلاد برای اهداف مختلف مورد استفاده قرار گرفته است.
تقاضای جهانی برای آنتیموان تحت سلطه مواد بازدارنده شعله و به دنبال آن باتری های اسید سرب است و انتظار می رود این روند در طول دوره پیش بینی ادامه یابد. افزایش تقاضا برای بازدارنده های شعله در انواع صنایع مصرف کننده نهایی، مانند پلاستیک، یکی از عوامل اصلی افزایش تقاضا برای آنتیموان بوده است. باتری های اسید سرب در صنایع مختلفی از جمله خودروسازی و کاربردهای دریایی استفاده می شوند. انتظار میرود افزایش تقاضا برای خودروهای الکتریکی باعث افزایش تقاضای آنتیموان شود. کالاهای مصرفی، مانند خودرو و منسوجات، صنایع مصرف کننده اصلی آنتیموان هستند. در نتیجه، عوامل اقتصاد کلان مانند رشد تولید ناخالص داخلی و برابری قدرت خرید، محرک های مهم رشد برای بازار آنتیموان هستند. قرار گرفتن در معرض آنتیموان می تواند باعث مشکلات سلامتی جدی مانند مشکلات تنفسی، تحریک پوست و سرطان ریه شود. آنتیموان همچنین چندین خطر زیست محیطی ایجاد می کند که منجر به افزایش تعداد مقررات برای تنظیم مصرف آنتیموان شده و رشد بازار آنتیموان را خفه می کند.



















