
عنصر نیوبیم (Niobium) با نماد شیمیایی Nb، یکی از عناصر شیمیایی جدول تناوبی است که عدد اتمی آن ۴۱ است. این عنصر در حقیقت چهل و یکمین عنصر جدول تناوبی بوده که در گروه VB و دوره پنجم جدول تناوبی قرار دارد. در واقع عنصر نیوبیوم یک فلز واسطه (Transition Metals) نرم به رنگ خاکستری روشن است. لازم به ذکر است که این عنصر با نام کلمبیم یا کلمبیوم (Columbium) با نماد شیمیایی Cb، نیز شناخته می شود. این فلز با عناصر وانادیم (V)، تانتالم (Ta) و دوبنیم (Db) در گروه پنج واسطه جدول تناوبی قرار گرفته است. در ادامه این مقاله در نشریه جهان شیمی فیزیک به بررسی عنصر نیوبیوم پرداخته می شود. لطفا با ما همراه باشید.
فهرست مطالب این مقاله
۱- تاریخچه کشف عنصر نیوبیم
۲- پیدایش و منابع عنصر شماره ۴۱ جدول تناوبی
۳- ویژگی های فیزیکی و شیمیایی عنصر نیوبیم
۴- ایزوتوپ های عنصر نیوبیم
۵- کاربرد های عنصر نیوبیم
۶- ترکیبات عنصر نیوبیوم
۷- خطرات نیوبیم بر روی سلامتی انسان
۸- طریقه نگهداری فلز نیوبیوم
تاریخچه کشف عنصر نیوبیم
واژه نیوبیوم به معنای دختر تانتالوس از کلمه یونانی نیوبه (Niobe) گرفته شده است. این عنصر برای اولین بار در سال ۱۸۰۱ میلادی، توسط چارلز هچت (Charles Hatchett) کشف شد. این دانشمند عنصر نیوبیم را از سنگ معدنی کلومبیت بدست آورد. به همین دلیل هچت، عنصر کشف شده را کلمبیوم نامگذاری کرد. این سنگ معدن در سال ۱۷۵۰ میلادی توسط جان وین تروپ (John Winthrop) به انگلستان ارسال شده بود.

در همان زمان سردرگمی های زیادی درباره خواص بسیار شبیه عناصر نیوبیوم و تانتالیوم وجود داشت. تا اینکه در سال ۱۸۴۶ میلادی، شیمیدان آلمانی هنریچ رز (Heinricht Rose) به همراه چـارلز مارگینت (Charles Marigance) دوباره این عنصر را کشف کردند. در حالیکه این دو دانشمند از کار های هچت و اکتشاف او اطلاعی نداشتند. از این جهت نام متفاوت نیوبیم را بر روی آن گذاشتند. بعد از آن و در همان سال، دانشمند سوئدی کریستین بلومسترند (Cristian Blomstarnd) با کمک روش کاهش کلرید نیوبیوم به وسیله حرارت دادن در اتمسفر هیدروژن توانست به عنصر نیوبیوم خالص دست پیدا کند.
نام نیوبیوم در سال ۱۹۵۰ میلادی در انجمن بین المللی شیمی محض و کاربردی به تصویب رسید. بدین صورت بسیاری از انجمن های شیمی و سازمان های دولتی نام رسمی نیوبیوم انجمن IUPAC را برای این عنصر بکار می برند. در مقابل، بسیاری دیگر از جمله فلز شناسان و تولید کنندگان آمریکایی هنوز نیز این فلز را با همان نام اصلی و قدیمی کلمبیم استفاده می کنند.
پیدایش و منابع عنصر شماره ۴۱ جدول تناوبی
عنصر نیوبیوم یک فلز نادر است که در طبیعت به عنوان یک عنصر آزاد پیدا نمی شود. در واقع عنصر نیوبیم در ترکیب با دیگر عناصر موجود در مواد معدنی می باشد. این عنصر در حقیقت سی و چهارمین عنصر رایج در پوسته زمین می باشد. بنابراین منبع اصلی این فلز، سنگ های معدنی است. از جمله کانی های اصلی آن می توان به کانی های کلمبیت، نیوبیت، تانتالیت- نیوبیت، یوزنیت و پاروکلر اشاره کرد. لازم به ذکر است که معادن بزرگ عنصر نیوبیم در واقع در سنگ های آذرین کربناتیت ها که خود از اجزا تشکیل دهنده کانی پاروکلر می باشند پیدا می شوند.
توجه داشته باشید که کانی های معدنی که دارای عنصر نیوبیوم هستند، معمولا دارای عنصر تانتالیم نیز می باشند. برای استخراج به صورت تجاری، فلز نیوبیوم را با تشکیل اولین اکسید (Nb۲O۵) استخراج می کنند. سپس اکسید مربوطه را با استفاده از کربن یا هیدروژن کاهش می دهند. ذکر این نکته خالی از لطف نیست که ذخایر بزرگ عنصر نیوبیم در کشور های کانادا، برزیل، نیجریه، کنگو و روسیه یافت می شود.

ویژگی های فیزیکی و شیمیایی عنصر نیوبیم
عنصر نیوبیوم، در واقع فلزی سفید مایل به خاکستری است. این فلز هادی جریان الکتریسیته می باشد. خصوصیات ویژه نیوبیم از ساختار اتمی آن ([۳۶Kr] ۴d۴۵s۲) ناشی می شود. همانطور که از آرایش الکترونی مشخص است، اوربیتال d لایه ماقبل آخر در این عنصر در حال پر شدن است. این عنصر به واسطه آرایش الکترونی که دارد، در دسته فلزات واسطه قرار می گیرد. فلزات واسطه در حقیقت بین فلزات قلیایی خاکی (گروه دوم) و عناصر گروه بور در جدول تناوبی قرار گرفته اند. به عناصر واسطه، عناصر گروه B نیز گفته می شود. با توجه به آرایش الکترونی مشخص است که پنج الکترون در دورترین لایه الکترونی آن وجود دارد. پس در ترکیبات شیمیایی حتی به صورت کاتیون پنج بار مثبت (+Nb ۵) نیز ظاهر می شود.
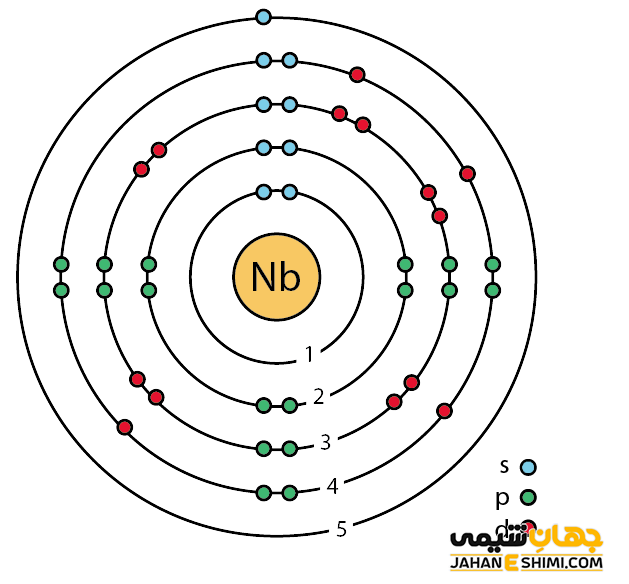
عنصر شماره ۴۱ جدول تناوبی، فلزی شکل پذیر و چکش خوار است. بنابراین خاصیت مفتول شدن را نشان می دهد. این فلز در دمای اتاق اکسید نمی شود و از جلا نمی افتد. حال اگر در دمای اتاق و برای مدت زمانی در معرض هوا باشد، به رنگ آبی کمرنگ در می آید. عنصر نیوبیوم در صورتیکه گرم شود می تواند با هالوژن ها و یا اکسیژن واکنش دهند (در دمای ۲۰۰ درجه در مجاورت هوا اکسید می شود). نکته قابل توجه اینست که حتی تا ۱۰۰ درجه سانتیگراد نیز، اسید نیتریک بر آن اثری ندارد. معمولا زمانیکه در معرض هوا قرار می گیرد، یک لایه اکسید بر روی آن تشکیل می شود. رنگ آن به ضخامت لایه اکسید تشکیل شده بستگی دارد. معمولا به رنگ سایه های آبی، سبز و زرد مشاهده شده است.
جالب است بدانید که
فلز نیوبیم در فشار جو، دارای بالاترین دمای بحرانی در عناصر ابر رسانا است. علاوه بر آن، این فلز یکی از سه عنصر ابر هادی نوع دوم می باشد. در واقع وانادیوم و تکنتیوم دو عنصر دیگر از این نوع هستند. این بدان معناست که اگر این عنصر در معرض میدان مغناطیسی قوی قرار گیرد، باز هم ابر هادی باقی خواهد ماند. دقت داشته باشید که خواص شیمیایی عنصر نیوبیوم شباهت زیادی به خصوصیات شیمیایی عنصر تانتالیوم دارد. عنصر تانتالیوم در جدول تناوبی در زیر عنصر نیوبیم قرار گرفته است. از طرفی دیگر، قابلیت شکل پذیری در آن مشابه فلز آهن است. از طرفی دیگر، فلز نیوبیوم یکی از پنج فلز اصلی با مقاومت بسیار بالا به گرما است. چهار فلز مقاوم دیگر عبارتند از : تنگستن، مولیبدن، تانتالم و رنیوم.
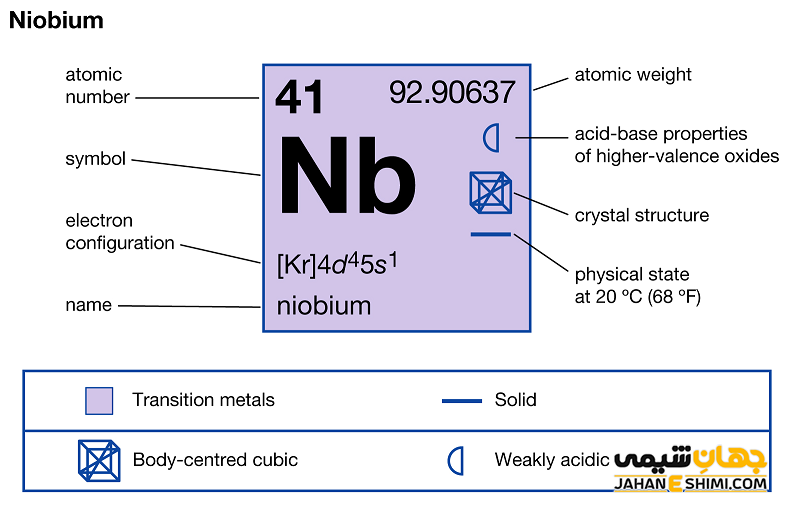
از دیگر ویژگی های عنصر نیوبیوم می توان به موارد زیر اشاره کرد.
- حالت فیزیکی آن در دمای ۲۵ درجه سلسیوس و فشار ۱ اتمسفر به صورت جامد است.
- دمای ذوب و دمای جوش این عنصر به ترتیب ۲۴۷۷ و ۴۷۴۴ درجه سانتی گراد است.
- عنصر نیوبیم در هوا به سرعت اکسید نمی شود.
- ساختار بلوری آن به شکل مکعبی مرکز پر (bcc) است.
- این عنصر آلوتروپ ندارد.
- جرم اتمی نیوبیم برابر با ۹۲.۹۰۶۳۸ g/mol است.
- چگالی آن نیز برابر با ۸.۵۷ g/cm۳ می باشد.
- یون های نیوبیم معمولا عدد اکسایش برابر با اعداد -۱، -۳، ۰، +۱، +۲، +۳، +۴ و +۵ را دارند. در حقیقت یک اکسید اسیدی ملایم محسوب می شود. اعداد اکسایش ۰ و +۵ متداول تر می باشند.
- انرژی یونیزاسیون آن برابر با ۶۵۲.۱ kJ/mol است.
ایزوتوپ های عنصر نیوبیم
همانطور که در مقالات پیشین نشریه جهان شیمی فیزیک بیان شده است، ایزوتوپ های یک عنصر، تنها در تعداد نوترون ها با هم تفاوت دارند. نیوبیم طبیعی تنها از یک ایزوتوپ پایدار ۹۳Nb (100 %) تشکیل شده است. علاوه بر آن، ۳۲ ایزوتوپ ناپایدار نیوبیوم نیز شناخته شده است. از جمله پایدار ترین رادیو ایزوتوپ های آن، می توان به ۹۲Nb با نیمه عمر ۷/۳۴ میلیون سال، ایزوتوپ رادیو اکتیوی ۹۴Nb با نیمه عمر ۲۰۳۰۰ سال و همچنین رادیو ایزوتوپ ۹۱Nb با نیمه عمر ۶۸۰ سال اشاره کرد. تعدادی رادیو ایزوتوپ دیگر نیز شناسایی شده اند که نیمه عمر بیشتر آنها کمتر از ۲ ساعت است.
کاربرد های عنصر نیوبیم
فلز نیوبیوم در تولید آلياژ های مغناطیسی ابر رسانا، موشک ها، جت ها، راکت ها و وسایل سرما زایی کاربرد گسترده ای دارد. به عنوان مثال، آلیاژ های نیوبیوم-تیتانیم و همچنین آلیاژ نیوبیوم- قلع جهت ساخت کابل های مغناطیسی ابرهادی که در حقیقت حالت مغناطیسی بالایی را تولید می کنند، بکار می روند. علاوه بر آن، این آلیاژ های ابررسانا در آهنربا های ابر رسانای اسکنر هایMRI ، دستگاه های رزونانس مغناطیسی هسته ای و شتاب دهنده های ذرات نیز استفاده می شوند. به همین دلایل می توان گفت که عنصر نیوبیوم یکی از مهمترین عناصر در جهان است.
اگر از مقدار قابل توجهی از فلز نیوبیوم به صورت خالص در نیکل، کبالت و آهن جهت ساخت آلیاژ های سنگین بهره ببرند؛ آلیاژ بدست آمده در اجزای موشک ها، موتور های جت و دیگر تجهیزاتی که به مقاومت بالا در مقابل گرما احتیاج دارند، استفاده می شود. به عنوان مثال در سیستم های پیشرفته ساختار فضایی، از این عنصر استفاده می کنند. عنصر نیوبیم در سایر آلیاژ ها نیز می تواند استفاده شود. در واقع در فلزات ضد زنگ و به عنوان آلیاژ فلزات غیر آهنی کاربرد دارد. این آلیاژ ها بسیار قوی می باشند. بنابراین اغلب جهت ساخت فلزات استیل مخصوص، خطوط لوله و اتصالات جوش خورده محکم بکار می روند. همچنین به عنوان عنصر پایدار کننده کاربید در فولاد های ضد زنگ و یا به عنوان عنصر استحکام زا در آلیاژ های پایه نیکل و کبالت در دما های بالا در نظر گرفته می شود.

جالب است بدانید که
به دلیل رنگ آبی نیوبیوم، این عنصر می تواند به عنوان آلیاژ در صنعت طلا و جواهرسازی استفاده شود. همچنین، در سایر جواهرات نیز به عنوان جایگزین ضد آلرژی برای عنصر نیکل بکار گرفته می شود. از طرفی دیگر، این فلز مقطع عرضی پایینی در برابر نوترون های گرمایی دارد. پس در صنایع هسته ای نیز کاربرد خواهد داشت. همچنین از آن می توان جهت جوشکاری طاق ها، میله های ضد زنگ و یا جوشکاری های قوسی به منظور تثبیت درجه فولاد زنگ نزن نیز استفاده کرد. نیوبیوم به عنوان یک جایگزین مناسب برای باطری ها و خازن ها کاربرد دارد. همچنین می توان این عنصر را به شیشه اضافه نمود تا یک ضریب شکست بیشتری را بدست آورد. در این صورت امکان داشتن شیشه های نازک تر و سبک تر را خواهید داشت.
از دیگر کاربرد های نیوبیوم می توان به الکترونیک (مثلا هارد دیسک های جدید)، اپتیک، راکتورهای اتمی، ساخت دستگاه های موج آکوستیکی سطحی، تلفن های همراه، مدولاتور های نوری، فرآیند سکه شناسی، ابزار برش، ساخت سیم های ولتاژ بالا، در سیستم های حفاظتی کاتدی در برخی از مخازن آب، ریل های جوش خوردنی و به عنوان یکی از مواد اصلی و مهم تشکیل دهنده کاتالیزور های ناهمگن با عملکرد بالا اشاره کرد.
ترکیبات عنصر نیوبیوم
همانطور که بیان شد اکسید نیوبیوم از مهمترین ترکیبات فلز نیوبیوم است. از دیگر ترکیبات معدنی آن می توان به موارد زیر اشاره کرد.
- اکسید نیوبیم (NbO)
- دی اکسید نیوبیم (NbO۲)
- پنتا اکسید دی نیوبیم (Nb۲O۵)
- هیدرید نیوبیم (NbH)
- دی هیدرید نیوبیم (NbH۲)
- تری کلرید نیوبیم (NbCl۳)
- تترا کلرید نیوبیم (NbCl۴)
- پنتا کلرید نیوبیم (NbCl۵)
خطرات نیوبیم بر روی سلامتی انسان
نیوبیم دارای ترکیباتی است که خوشبختانه بیشتر مردم با آنها تماسی ندارند. به عبارت دیگر، نیوبیوم هیچ نقش بیولوژیکی نیز ندارد. اما توجه داشته باشید که تعدادی از این ترکیبات بسیار سمی می باشند، پس باید با احتیاط از آنها استفاده نمود. غبار این فلز برای پوست و یا چشم ها خطرناک است و قابل اشتعال می باشد. از طرفی دیگر، زمانیکه استنشاق شود، می تواند در ریه و استخوان ها باقی بماند. در این صورت با کلسیم وارد واکنش شده و سپس به عنوان فعال کننده سیستم آنزیمی عمل خواهد کرد. به عنوان نمونه، استنشاق چهل میلی گرم نیترید و یا پنتاکسید نیوبیم در متر مکعب در جانوران آزمایشگاهی سبب زخم شدن ریه ها می گردد. دقت داشته باشید که این عنصر بر روی محیط زیست اثر منفی نمی گذارد.

طریقه نگه داری فلز نیوبیوم
برای نگهداری فلز نیوبیوم حتی در دمای معمولی، باید حتما در یک فضای محافظت شده قرار داده شود. علاوه بر آن، پودر نیوبیوم را نیز بایستی در مخازن محکم و در بسته و در مکانی خنک، خشک، با تهویه مناسب و به دور از حرارت، گرما، شعله و جرقه نگهداری شود. لازم به ذکر است که برای خاموش کردن فلز نیوبیم در حال سوختن، به هیچ وجه از آب استفاده نکنید. زیرا در این صورت ممکن است باعث انفجار بزرگ شود.



















