
در علم شیمی، نظریه برخورد (Collision theory)، به بررسی برخورد میان ذرات مختلف با یکدیگر می پردازد. این نظریه در واقع چگونگی انجام واکنش های شیمیایی و علت تغییر سرعت آنها را بیان می کند. علاوه بر آن، راه هایی نیز جهت تغییر در سرعت واکنش های شیمیایی پیشنهاد می دهد. توجه داشته باشید که بسیاری از سوالات مربوط به قوانین برخورد را می توان به کمک قوانین بقا جواب داد. در مقالات پیشین نشریه جهان شیمی فیزیک، درباره واکنش های شیمیایی مطالبی گفته شده است. در این مقاله به مفهوم نظریه برخورد و عوامل موثر بر آن پرداخته می شود. لطفا همراهی بفرمایید.
فهرست مطالب این مقاله
۱- سینتیک شیمیایی شیمی دوازدهم
۲- نظریه برخورد
۳- شرط انجام واکنش در نظریه برخورد
۱-۳- تعداد برخورد ها
۲-۳- جهت گیری مناسب ذرات در هنگام برخورد
۳-۳- انرژی مناسب و کافی ذرات در هنگام برخورد
۴- توضیح عوامل موثر بر سرعت واکنش به کمک نظریه برخورد
۱-۴- اثرات دما
۲-۴- اثر غلظت
۳-۴- اثر فشار
۴-۴- اثر کاتالیزور
۵- ایراد های نظریه برخورد
فهرست مطالب
سینتیک شیمیایی شیمی دوازدهم
نظریه های سینتیک شیمیایی به طور کلی به دو دسته نظریه حالت گذار و نظریه برخورد طبقه بندی می شوند. با وجود اینکه اساس هر دو نظریه، برخورد میان ذرات واکنش دهنده ها است، اما تفاوت های بنیادی بین آنها وجود دارد. این تفاوت ها عبارتند از :
- نظریه برخورد تنها برای واکنش های انجام شده در فاز گازی به کار می رود، در صورتیکه نظریه حالت گذار علاوه بر فاز گازی در فاز محلول نیز کاربرد دارد.
- در نظریه برخورد ذرات واکنشگر را به صورت گوی هایی سخت در نظر می گیرند، در حالیکه در نظریه حالت گذار این ذرات ضمن مبادله انرژی، بر یکدیگر نیز اثر می گذارند.
- در نظریه برخورد تنها حرکات انتقالی ذرات را در نظر می گیرند، اما در نظریه حالت گذار حرکات چرخشی و ارتعاشی ذرات واکنش دهنده نیز در چگونگی انجام واکنش تاثیر گذار هستند.
- در نظریه برخورد بعد از برخورد موثر، واکنش انجام می شود، در حالیکه در نظریه حالت گذار، واکنشگر ها پس از برخورد در کنار یکدیگر قرار گرفته و ترکیبات پیچیده فعال یا کمپلکس ها تشکیل می شوند.
- در نظریه برخورد، انرژی فعال سازی وجود دارد اما نمی توان مقدار آن را محاسبه کرد، در حالیکه مقدار انرژی فعال سازی را در نظریه حالت گذار می توان محاسبه نمود.
- در نظریه برخورد هیچ حالت گذاری وجود ندارد.
نکته مهم
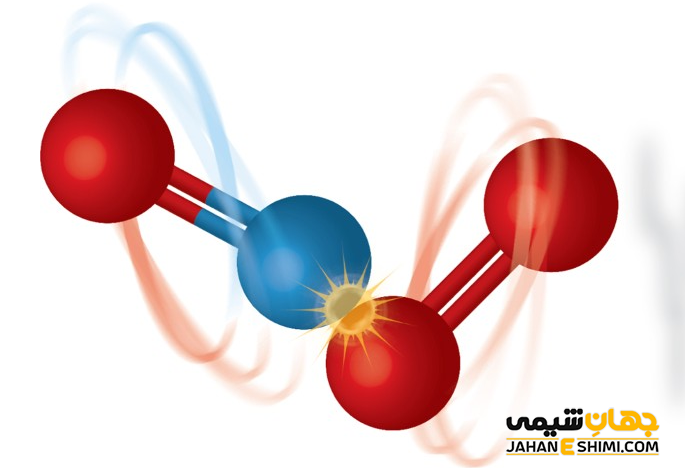
در نظریه حالت گذار، زمانیکه ذرات واکنش دهنده با یکدیگر برخورد کنند، این ذرات مدت زمانی در کنار هم قرار می گیرند. در این صورت پیوند های موجود دگرگون شده، پس سست می شوند و در نتیجه پیوند های جدید ایجاد می گردند. به این حالت که در آن، پیوند های اولیه در حال شکستن شدن و پیوند های جدید در حال تشکیل شدن باشند، حالت گذار یا پیچیده فعال گفته می شود. این حالت گذار دارای ویژگی های ویژه ای می باشد که عبارتند از :
- محتوای انرژی حالت گذار در مقایسه با مواد اولیه و محصولات بیشتر است.
- به دلیل داشتن سطح انرژی زیاد، حالت گذار پایداری بسیار کمی دارد، بنابراین می توان گفت این حالت اصلا وجود خارجی ندارد.
- حالت گذار هم به واکنش دهنده ها و هم به فرآورده ها شبیه است.
- تشکیل حالت گذار با مصرف انرژی و از بین رفتن آن با آزاد شدن انرژی همراه خواهد بود.
نظریه برخورد
این نظریه به طور مستقل توسط دو دانشمند، یک شیمیدان آلمانی به نام مکس تراتز (Max Trautz) در سال ۱۹۱۶ و یک پروفسور شیمی انگلیسی به نام ویلیام لوئیس (William Lewis) در سال ۱۹۱۸ ارائه شده است. همانطور که بیان شد، بسیاری از مسائل مربوط به قوانین برخورد را می توان به کمک قوانین بقا حل نمود. از آنجاییکه قوانین بقا علاوه بر مکانیک کلاسیک، در مکانیک کوانتومی نیز معتبر اند، بنابراین نتایج حاصله از این قوانین در مورد ذراتی با اندازه های بسیار کوچک مانند اتمی و یا حتی زیر اتمی نیز معتبر می باشد.
در حقیقت برخورد را با توجه به نوع و اندازه ذرات برخورد کننده می توان بررسی نمود. در هنگامیکه دو ذره با اندازه های بزرگ با هم برخورد کنند، برخورد و در نتیجه تماس ذرات با یکدیگر کاملا رخ می دهد، در حالیکه، در برخورد ذرات کوچک و باردار، اصلا تماسی میان ذرات نخواهد بود. در این حالت، ذرات باردار در اثر نیرو هایی که به هم وارد می کنند، از کنار هم دور می شوند. از این رو می توان گفت که در حالت کلی برخورد را می توان از دو دیدگاه مختلف مکانیک کلاسیک و مکانیک کوانتومی مورد مطالعه و بررسی قرار داد. دقت داشته باشید که انواع برخورد در مکانیک کلاسیک به سه دسته برخورد الاستیک، برخورد غیرالاستیک و برخورد غیرالاستیک کامل تقسیم می شود. توضیح کامل درباره این نوع برخورد ها از حوصله این بحث خارج است.
جالب است بدانید که
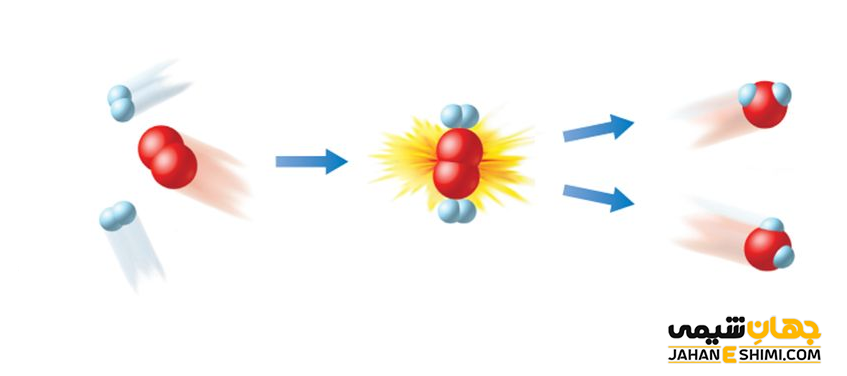
این نظریه و همچنین سرعت واکنش های شیمیایی به وسیله این واقعیت اساسی بکار می روند که تمام واکنش های شیمیایی نتیجه برخورد میان اتم ها، مولکول ها یا یون ها می باشند. در حقیقت بر طبق این نظریه، برخورد بین ذرات، باعث ایجاد واکنش شیمیایی میان آنها می شود که می تواند منجر به شکستن برخی از پیوند ها و ایجاد پیوند های شیمیایی جدید شود. بدین شکل، محصولات جدیدی تشکیل خواهد شد. علاوه بر آن، این نظریه می تواند توضیح دهد که چرا واکنش های شیمیایی مختلف و متنوع با سرعت های متفاوتی انجام می شوند. در واقع به کمک این نظریه می توان سرعتی که در آن، یک واکنش اتفاق می افتد را پیش بینی نمود. همچنین با دانستن شرایط اولیه واکنش، می توان گفت که فرآورده ها تا چه میزان آهسته و یا سریع ممکنست در یک واکنش شیمیایی، تولید شوند.
شرط انجام واکنش در نظریه برخورد
واکنش شیمیایی فوق را در نظر بگیرید :
A + B → محصولات
بر اساس نظریه برخورد، اگر قرار باشد میان مولکول های A و B واکنشی انجام شود، در ابتدا این مولکول ها باید به اندازه ای به هم نزدیک شوند که تعدادی از پیوند های شیمیایی آنها شکسته و به طور همزمان پیوند های شیمیایی جدید جهت تولید محصولات تشکیل شود. به این فرآیند، برخورد گفته می شود.
بنابراین همانطور که بیان شد، جهت شروع هر واکنش شیمیایی، ذرات واکنش دهنده باید با یکدیگر برخورد مناسب داشته باشند. اما توجه داشته باشید که فقط تعداد محدودی از برخورد ها منجر به تغییرات شیمیایی و انجام واکنش می شوند. به این برخورد ها، برخورد های مؤثر گفته می شود. برخوردی موثر خواهد بود که در هنگام تماس با سایر ذرات، انرژی فعال سازی مورد نیاز جهت شکستن پیوند های موجود را داشته باشد و بتواند پیوند های جدیدی تشکیل دهند. حاصل آن، محصولات واکنش خواهند بود. یک برخورد موثر و کارا دارای سه ویژگی زیر است :
- تعداد برخورد ها
- جهت گیری مناسب ذرات در هنگام برخورد
- انرژی مناسب و کافی ذرات در هنگام برخورد
تعداد برخورد ها
بر طبق نظریه برخورد، سرعت یک واکنش شیمیایی به تعداد برخورد های میان ذرات واکنش دهنده در واحد حجم و زمان بستگی دارد. در واقع با افزایش غلظت ذرات واکنش دهنده، تعداد برخورد ها در واحد حجم و همچنین در واحد زمان بیشتر می شود، بنابراین، تعداد برخورد های موثر نیز افزایش پیدا کرده و واکنش سریع تر انجام می شود.
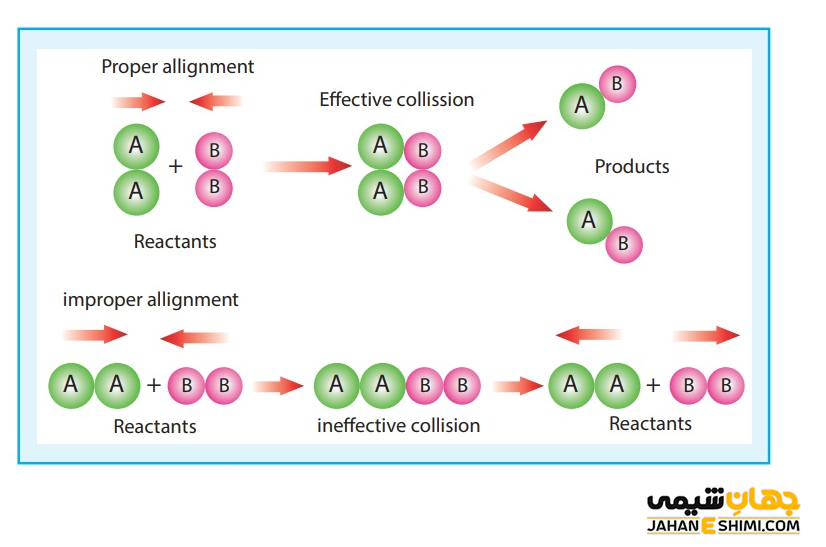
جهت گیری مناسب ذرات در هنگام برخورد
برخورد در صورتی انجام می گیرد که ذرات واکنش دهنده بتوانند از جهت مناسبی به یکدیگر نزدیک شوند. جهت تشخیص یک برخورد مناسب و موثر، بایستی در ابتدا فرمول ها و ساختار لوئیس واکنش دهنده ها و همچنین فرآورده ها را بررسی نمود. در این صورت می توان دید که چه پیوند هایی باید شکسته و یا حتی تشکیل شوند. توجه داشته باشید که میان اتم هایی از واکنشگر ها که قرار است با یکدیگر پیوند شیمیایی تشکیل بدهند باید برخورد صورت پذیرد.
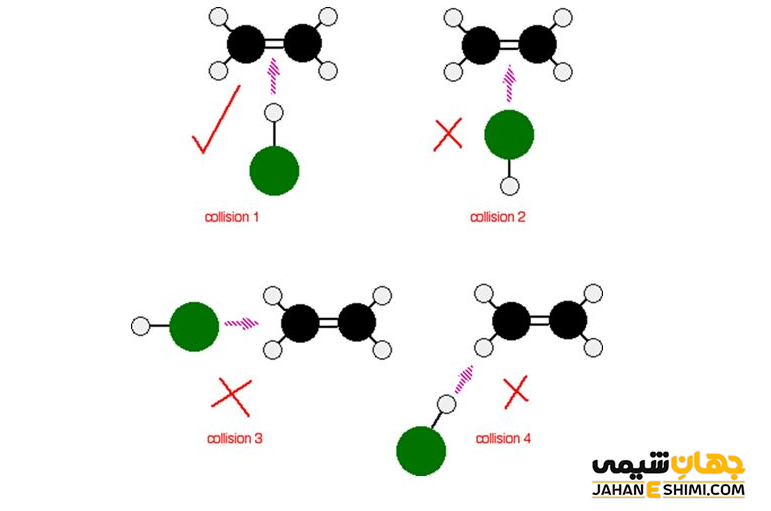
انرژی مناسب و کافی ذرات در هنگام برخورد
در هنگام برخورد میان ذرات واکنش دهنده، این ذرات باید انرژی کافی داشته باشند تا پیوندهای اولیه و قدیمی شکسته شوند. حداقل انرژی لازم جهت شروع یک واکنش شیمیایی را انرژی فعال سازی یا اکتیواسیون می گویند. در صورتی یک برخورد، نتیجه بخش خواهد بود که واکنشگر ها از این حداقل انرژی برخوردار باشند. در حقیقت شکستن پیوند های شیمیایی قدیمی نیازمند انرژی از برخورد ها می باشد. در حالیکه ایجاد پیوند های شیمیایی جدید، انرژی را به شکل گرما آزاد می کند. از این رو، انرژی فعال سازی به انرژی مورد نیاز برای شکستن پیوند های قدیمی و تشکیل پیوند های جدید گفته می شود. لازم به ذکر است که از دیدگاه انرژی دو نوع برخورد می توان در نظر گرفت :
- برخورد آهسته : در این نوع برخورد، دو ذره با یکدیگر برخورد می کنند، اما دافعه ابر الکترونی اتم ها باعث می شود که آنها از هم دور شوند.
- برخورد شدید : در این نوع برخورد، دو ذره با یکدیگر برخورد می کنند، اما ابر های الکترونی اتم ها در یکدیگر نفوذ کرده و در نهایت پیوند جدیدی تشکیل می شود.
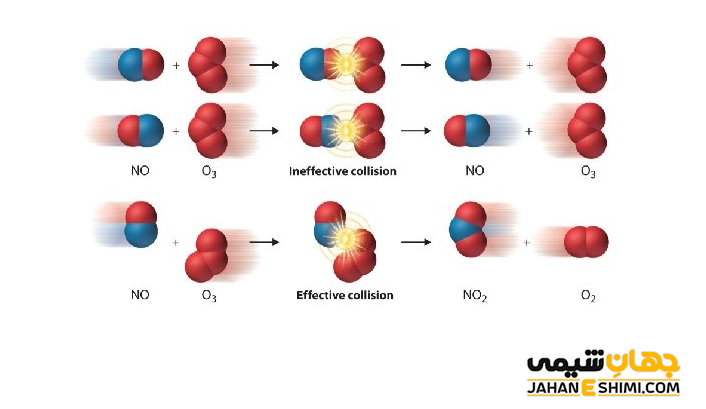
مثال
با توجه به نظریه برخورد، بیان کنید که در واکنش زیر، برخورد موثر و مناسب چگونه انجام می شود؟
2ClO (g) → Cl۲ (g) + O۲ (g)
با توجه به محصولات مشخص می شود که در این واکنش، پیوند های Cl-Cl و O=O باید تشکیل گردد، بنابراین بایستی همزمان برخورد میان دو اتم اکسیژن و دو اتم کلر انجام شود.
توضیح عوامل موثر بر سرعت واکنش به کمک نظریه برخورد
عواملی همچون دما، غلظت، فشار و کاتالیزور بر روی سرعت یک واکنش شیمیایی موثر می باشند. در ادامه مقاله به بررسی این عوامل پرداخته می شود.
اثر دما
زمانیکه واکنشگر ها حرارت ببینند، مرتعش می شوند و در نتیجه با شدت بیشتری با سایر واکنش دهنده ها برخورد می کنند. این اتفاق، سرعت واکنش شیمیایی را افزایش داده و باعث عملکرد بهتر آن می شود. به عبارت دیگر، با افزایش دما، تعداد برخورد ها بیشتر می شود و در نتیجه تعداد برخورد های موثر و کارا نیز افزایش پیدا می کند و واکنش سریع تر انجام خواهد شد.
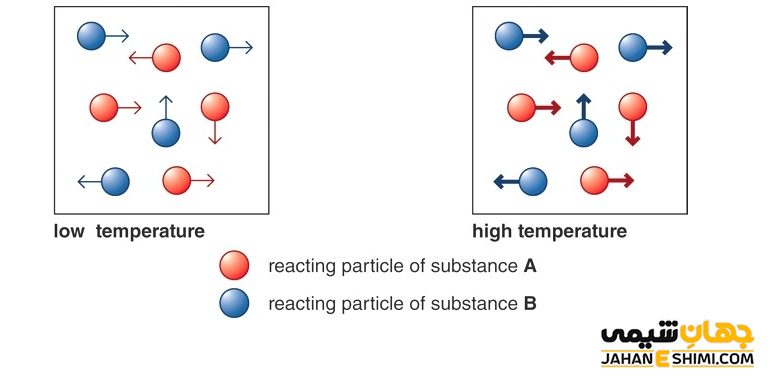
اثر غلظت
همان گونه که می دانید غلظت در واقع تعداد مولکول های واکنشگر ها در واحد حجم می باشد. بنابراین با افزایش غلظت واکنش دهنده ها، تعداد آنها نیز زیاد می شود و باعث بیشتر شدن احتمال برخورد میان آنها می گردد. به بیان دیگر، تعداد برخورد های میان مولکول های واکنش دهنده ها با غلظت هر کدوم از آنها متناسب است.
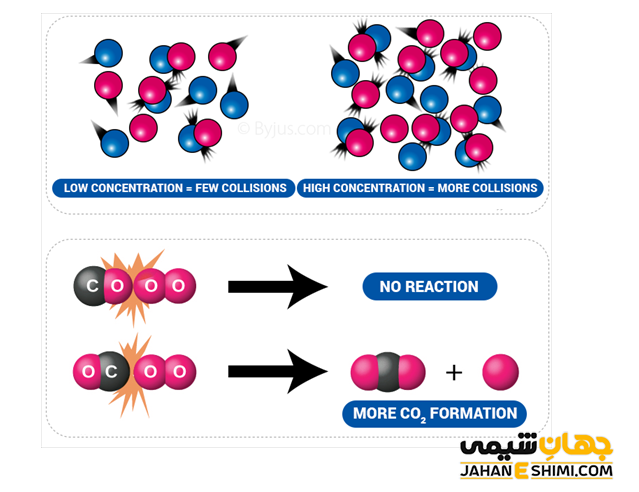
اثر فشار
اگر واکنش شیمیایی مورد نظر در فاز گازی انجام شود، با افزایش فشار و در نتیجه فشرده سازی گاز، به صورت خودکار سبب افزایش غلظت گاز خواهد شد. این امر باعث می شود که احتمال برخورد واکنش دهنده های گازی بیشتر شود و در نهایت سرعت واکنش نیز افزایش یابد.
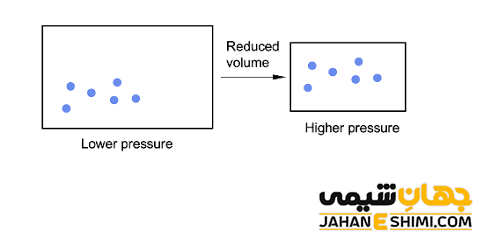
اثر کاتالیزور
بر اساس نظریه برخورد، با افزودن کاتالیست، انرژی فعال سازی کمتری برای انجام واکنش شیمیایی در برخورد بین ذرات نیاز خواهد بود. در واقع کاتالیزور با مولکول های واکنشگر برخورد می کند، پس انرژی کمتری برای تغییر شیمیایی نیاز دارد. در این صورت، تعداد بیشتری از برخورد ها انرژی مورد نیاز جهت انجام واکنش شیمیایی را خواهند داشت و در نتیجه، سرعت واکنش افزایش پیدا می کند.
ایراد های نظریه برخورد
در نظریه برخورد، ذرات را جداگانه و مستقل از یکدیگر در نظر می گیرند، بنابراین این فرض تنها در فاز گازی صادق است. از این رو، نظریه برخورد در سایر فاز ها (مانند فاز های محلول، جامد یا مایع) قابل استفاده نمی باشد. همان طور که بیان شد، در این نظریه، ذرات واکنشگر را به شکل گوی های سخت در نظر می گیرند که برخورد هایی کشسان دارند. توجه داشته باشید که برخوردی کشسان است که در طی آن هیچ انرژی برای تغییر شکل ساختار گوی ها صرف نشود. لازم به ذکر است که برخورد میان اتم ها کشسان نمی باشد، زیرا اتم ها بر هم اثر می گذارند مثل هم پوشانی در پیوند های کووالانسی.
همچنین در نظریه برخورد فقط حرکات انتقالی ذرات را در نظر می گیرند و در واقع به تاثیر حرکات چرخشی و ارتعاشی در واکنش ها توجه نشده است. در حالیکه می دانید علاوه بر حرکت انتقالی، حرکات چرخشی و ارتعاشی نیز مهم می باشند. همچنین این نظریه، قادر به اندازه گیری و محاسبه مقدار انرژی فعال سازی نمی باشد.



















